Endothelinrezeptorantagonisten: Endothelin-1(ET-1) ist ein potenter Vasokonstriktor und Stimulator der pulmonalen Arteriellenzahnmuskelzellproliferation. Plasmaspiegel von ET-1 sind korreliertmit erhöhter Schwere und verschlechterterter Prognose von PAH. Endothelinrezeptorantagonisten, wie Bosentan(Tracleer) und Ambrisentan (Letairis), arbeiten durch kompetitive Hemmung von ET-1 von Bindungendothelinrezeptoren, um den Lungengefäßwiderstand zu verringern.,Es wurde gezeigt, dass 14 Bosentan mehr Arzneimittelwechselwirkungen hat als Ambrisentan.31 Cyclosporin ist mit Bosentan kontraindiziert, und Wirksamkeit der hormonellen Kontrazeption kann mit Bosentan reduziert werden.32,33 Die gleichzeitige Anwendung von Bosentan und Glyburid ist aufgrund ihres CYP3A4-induzierenden Potenzials ebenfalls kontraindiziert, was zu einem erhöhten Plasmalevel beider Arzneimittel führt.32,34 Wenn Bosentan und Sildenafil gleichzeitig verabreicht werden, können die Bosentanspiegel ansteigen und die Sildenafilspiegel sinken, obwohl möglicherweise keine Dosisanpassungen erforderlich sind.,Bis heute ist Ambrisentan mit einer klinisch signifikanten Wechselwirkung verbunden. Bei Anwendung mit Cyclosporin sollte Ambrisentan auf 5 mg täglich begrenzt werden.35,36
Angesichts des Risikos für Leberschäden und teratogene Schäden(Schwangerschaftskategorie X) sind Bosentan und Ambrisentan nur verfügbardurch das Tracleer Access-Programm bzw.32,36
Prostanoide: Die Prostacyclinsynthase ist bei Patienten mit PAH reduziert. Infolgedessen besteht eine unzureichende Produktion von Prostacyclin (PGI2), einem Vasodilatator mit antiproliferativer Wirkung.,14 Patienten mit PAH werden mit Prostanoiden behandelt, um das Prostacyclin innerhalb des pulmonalen arteriellen Gefäßsystems zu ersetzen.37 Prostanoide induzieren pulmonale arterielle Vasodilatation, behindern das Wachstum glatter Muskelzellen und stören die Thrombozytenaggregation.37
Es stehen mehrere Prostanoide zur Verfügung. Iloprost (Ventavis) wird mit dem I-neb AAD-System oder dem Prodose AAD-System inhaliert.37,38 Treprostinil (Tyvaso) ist ein weiteres Prostanoid, das Durchinhalation verabreicht werden kann. Bis heute gibt es keine pharmakokinetischen Studien mit Inhalationtreprostinil., Das Wirkstoffwechselwirkungspotenzial basiert auf dem, was bekannt istmit oralem oder injiziertem Treprostinil (Remodulin). Prostanoide verfügbarfür die parenterale Verabreichung umfassen Epoprostenol (Generikum, Flolan,Veletri) und Trepostinil (Remodulin). Epoprostenol wird aufgrund seiner kurzen Halbwertszeit von 2,7 Minuten als acontinuous IV Infusionspumpe abgegeben.39Es war das erste weit verbreitete Prostanoid und es wurde gezeigt, dass es die Lungenarterien effektiv erweitert, die Symptome von PAH reduziert und den Überlebensvorteil bietet.,37 Treprostinil kann als intravenöse Infusion oder als intravenöse Infusion bei Patienten verabreicht werden, bei denen eine intolerable Reizung durch SC-Verabreichung auftritt. Dosierungsanpassung vontrepostinil kann notwendig sein, wenn es mit Gemfibrozil orrifampin verwendet wird.40,41
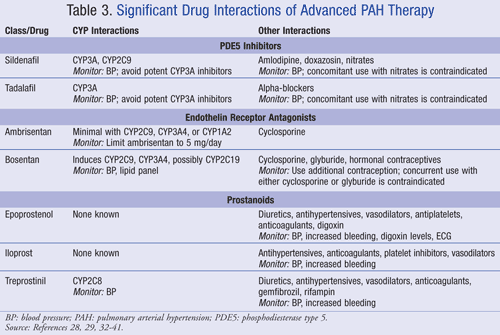
Eine Zusammenfassung der Arzneimittelwechselwirkungen fortgeschrittener Behandlungen für PAH ist in TABELLE 3.28,29,32-41
Rolle des Apothekers
Die Behandlung von PAH beinhaltet ein kompliziertes Medikamentenregime., Apotheker im Krankenhaus und in der Gemeinschaft können helfenpatienten verstehen die Notwendigkeit für verschiedene Arten von Medikamenten und elektropharmakologischen Therapien. Durch die geeignete Anwendung von Informationen aus Paketkennzeichnungen, Medikamentendatenbanken, Postmarketing-Berichten und FDAMedWatch-Hinweisen können Apotheker bei der Bestimmung der Klinischenrelevanz von Arzneimittelwechselwirkungen von PAH-Therapien und der Notwendigkeit von Arzneimittelanpassungen behilflich sein. Apotheker können auch andere Medikamente in den Pharmakotherapieplan integrieren.
Obwohl PAH eine seltene und tödliche Krankheit ist, hat sich die Prognose durch die Erweiterung der therapeutischen Möglichkeiten verbessert., Neue Medikamente sind inEntwicklung, wie Selexipag (ACT-293987).42 Apothekermit spezialisiertem Wissen über Medikamente sind gut positioniert, um die Arzneimittelüberwachung zu verbessern, die unerwünschte Ereignisse verhindern und letztendlich die Patientenversorgung optimieren kann.
1. Badesch DB, Abman SH, Simonneau G, et al. Medicaltherapy für pulmonale arterielle Hypertonie: aktualisierte ACCP evidenzbasiertklinische Praxisrichtlinien. Brust. 2007;131:1917-1928.
2. Höper MM. Definition, Klassifikation und Epidemiologie der pulmonalen arteriellen Hypertonie. Semin Respir Crit Care Med. 2009;30:369-375.
3., Frost AE, Badesch DB, Barst RJ, et al. Das veränderte Bild von Patienten mit pulmonaler arterieller Hypertonie in den Vereinigten Staaten: Wie unterscheidet es sich von historischen und Nicht-US-Zeitgenossenregistern? Brust. 2011;139:128-137.
4. Galie N, Höper MM, Humbert M, et al. Richtlinien für die Diagnose und Behandlung von pulmonaler Hypertonie. Eur Herz J. 2009; 30: 2493-2537.
5. Badesch DB, Raskob GE, Elliott CG, et al. Pulmonaryarterielle Hypertonie: Basismerkmale aus der REVEALregistry. Brust. 2010;137:376-387.
6. Simonneau G, Robbins IM, Beghetti M, et al., Aktualisierte klinische Klassifikation der pulmonalen Hypertonie. J Am Coll Cardiol. 2009;54(suppl 1):S43-S54.
7. Yuan JX, Rubin LJ. Pathogenese der pulmonalen arteriellen Hypertonie: die Notwendigkeit für mehrere Treffer. Durchblutung. 2005;111:534-538.
8. Lane KB, Machado RD, Pauciulo MW, et al. Heterozygotedermlinmutationen in BMPR2, die einen TGF-Beta-Rezeptor kodieren, verursachenfamiliale primäre pulmonale Hypertonie. Nat Genet 2000;26:81-84.
9. Deng Z, Morse JH, Slager SL, et al. Familiäre primärpulmonale Hypertonie (Gen PPH1) wird durch Mutationen im knochenmorphogenetischen Proteinrezeptor–II-Gen verursacht., Am J Hum Genet. 2000;67:737-744.
10. Girerd B, Montani D, Coulet F, et al. Klinischeergebnisse der pulmonalen arteriellen Hypertonie bei Patienten mit anACVRL1 (ALK1) – Mutation. Am J Respir Crit Care Med. 2010;181:851-861.
11. Harrison RE, Berger R, Haworth SG, et al. Transforminggrowth Factor-Beta-Rezeptor-Mutationen und pulmonale Arterienhypertension in der Kindheit. Durchblutung. 2005;111:435-441.
12. Gurney AM, Joshi S, Manoury B. KCNQ Kaliumkanäle:neue Ziele für Lungenvasodilatatoren? Adv Exp Med Biol. 2010;661:405-417.
13. Kuhr FK, Smith KA, Song MY, et al., Neue Mechanismen der pulmonalen arteriellen Hypertonie: Rolle der Ca2+ – Signalgebung. Am J Physiol Herz Circ Physiol. 2012;302:H1546-H1562.
14. McLaughlin VV, Archer SL, Badesch DB, et al. ACCP/AHA 2009 expert consensus document on pulmonary hypertension. J Am Coll Cardiol. 2009;53:1573-1619.
15. Coumadin (Warfarin) Packungsbeilage. Princeton, NJ: Bristol-Myers Squibb Co, Oktober 2011.
16. Rubin LJ. Primäre pulmonale Hypertonie. N Engl J Med. 1997;336:111-117.
17. Bumex (Bumetanide) Packungsbeilage. Parsippany, NJ. Datenzentren Validus erworben Pharmaceuticals LLC, September 2009.
18., Lasix (furosemide) package insert. Bridgewater, NJ: Sanofi-Aventis LLC; August 2011.
19. Demadex (torsemide) package insert. Somerset, NY: Meda Pharmaceuticals, Inc; February 2010.
20. Aldactone (spironolactone) package insert. New York, NY: Pfizer, Inc; January 2008.
21. Micromedex . GreenwoodVillage, CO: Truven Health Analytics, Inc. Updated periodically.www.micromedexsolutions.com. Accessed March 16, 2013.
22. Lexicomp . Hudson, OH:Lexi-Comp, Inc. Updated periodically. http://online.lexi.com. AccessedMarch 16, 2013.
23. Pitt B, Zannad F, Remme WJ., Die Wirkung von Spironolacton auf Morbidität und Mortalität bei Patienten mit schwerer Herzinsuffizienz. N Engl J Med. 1999:341:709-717.
24. Digoxin-Packungsbeilage. Columbus, OH: Roxane Laboratories, Inc; September 2012.
25. Procardia XL (Nifedipin) Packungsbeilage. New York: Pfizer, Inc; August 2011.
26. Cardizem (Diltiazem) Packungsbeilage. Bridgewater, NJ: BTA Pharmaceuticals, Inc; November 2009.
27. Norvasc (Amlodipin) Packungsbeilage. Research Triangle Park, NC: Synthon Pharmaceuticals, Inc; September 2007.
28. Revatio (Sildenafil) Packungsbeilage., New York: Pfizer Inc.; August 2012.
29. Adcirca (Tadalafil) Packungsbeilage. Indianapolis, IN: Eli Lilly and Company; im März 2012.
30. Muirhead GJ, Wulff MB, Fielding A, et al. Pharmakokinetische Wechselwirkungen zwischen sildenafil und saquinavir/ritonavir. Br J Clin Pharmacol. 2000;50:99-107.
31. Weiss J, Herzog M, Haefeli WE. Differentialmodulationder Expression wichtiger arzneimittelmetabolisierender Enzyme Undtransporter durch Endothelin-1-Rezeptorantagonisten Ambrisentan Undbosentan in vitro. Eur J Pharmacol. 2011;660:298-304.
32. Tracleer (bosentan) Packungsbeilage., South San Francisco, CA: Actelion Pharmaceuticals; Oktober 2012.
33. Treiber Ein, Schneiter R, Hausler S, et al. Bosentan ist asubstrat von menschlichem OATP1B1 und OATP1B3: Hemmung der Leberaufnahme alsder gemeinsame Mechanismus seiner Wechselwirkungen mit Cyclosporin A,Rifampicin und Sildenafil. Drogen-Metabene. 2007;35:1400-1407.
34. van Giersbergen PL, Treiber Ein, Clozel M, et al. Invivo-und In-vitro-Studien untersuchen die pharmakokinetische Wechselwirkungzwischen Bosentan, einem dualen Endothelinrezeptorantagonisten, und Glyburid. Clin Pharmacol Ther. 2002;71:253-262.
35. Frampton JE. Ambrisentan., Am J Cardiovasc Drugs. 2011;11:215-226.
36. Letairis (ambrisentan) Packungsbeilage. Foster City, CA: Gilead Sciences, Oktober 2012.
37. Bischof BM, Mauro VF, Khouri SJ. Praktische Überlegungen zur Pharmakotherapie der pulmonalen arteriellen Hypertonie. Pharmakotherapie. 2012;32:838-855.
38. Ventavis (iloprost Inhalationslösung) Packungsbeilage. South San Francisco, CA: Actelion Pharmaceuticals; August 2012.
39. Veletri (Epoprostenol zur Injektion) Packungsbeilage. South San Francisco, CA: Actelion Pharmaceuticals, Juni 2012.
40., Tyvaso (Trepostinil Inhalationslösung) packageinsert. Research Triangle Park, NC: United Therapeutics Corp; February2011.
41. Remodulin (Trepostinil injection) Packungsbeilage. Research Triangle Park, NC: United Therapeutics Corp; Februar 2011.
42. Selexipag (ACT-293987) in pulmonaler Arterienhypertension, GRIPHON-Studie. ClinicalTrials.gov.http://clinicaltrials.gov/show/NCT01106014. Zugriff auf September 16, 2013.
















Schreibe einen Kommentar