När temperaturen ökar gör också enzymreaktionshastigheten. En tio graders Celsius temperaturökning ökar aktiviteten hos de flesta enzymer med 50% till 100%. Variationer i reaktionstemperaturen så liten som 1 eller 2 grader kan införa förändringar på 10% till 20% i resultaten. Denna ökning är bara upp till en viss punkt tills den förhöjda temperaturen bryter enzymets struktur. När enzymet denatureras kan det inte repareras., Eftersom varje enzym är annorlunda i sin struktur och bindningar mellan aminosyror och peptider är temperaturen för denaturering specifik för varje enzym. Eftersom de flesta djurenzymer snabbt denatureras vid temperaturer över 40 ° C, utförs de flesta enzymbestämningar något under den temperaturen.
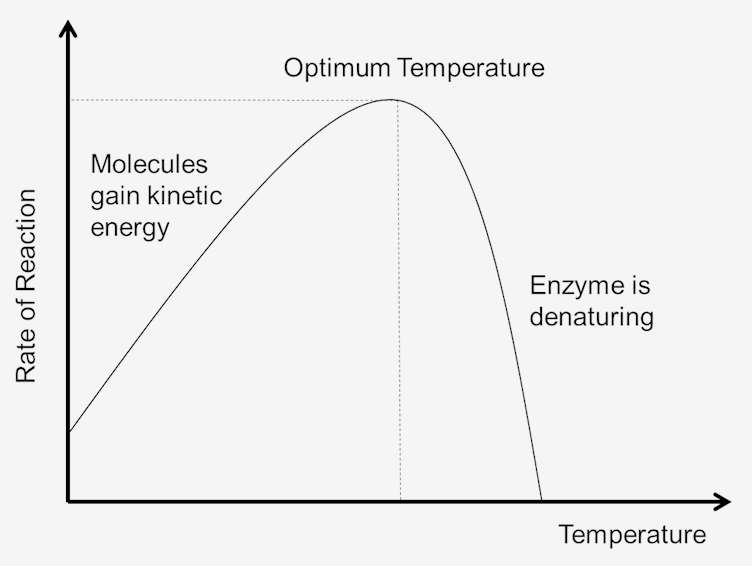 Figur 1. Effekt av temperaturen på reaktionshastigheten.
Figur 1. Effekt av temperaturen på reaktionshastigheten.
under en tidsperiod kommer enzymer att avaktiveras vid jämn måttliga temperaturer. Lagring av enzymer vid 5 ° C eller under är i allmänhet den mest lämpliga. Lägre temperaturer leder till långsammare kemiska reaktioner., Enzymer kommer så småningom att bli inaktiva vid frystemperaturer men kommer att återställa det mesta av deras enzymaktivitet när temperaturerna ökar igen, medan vissa enzymer förlorar sin aktivitet när de fryses.
kinetisk energi och inre energi
temperaturen hos ett system är till viss del ett mått på molekylernas kinetiska energi i systemet. Kollisioner mellan alla molekyler ökar när temperaturen ökar. Detta beror på ökningen av hastighet och kinetisk energi som följer temperaturökningar. Med snabbare hastigheter kommer det att finnas mindre tid mellan kollisioner., Detta resulterar i att fler molekyler når aktiveringsenergin, vilket ökar reaktionshastigheten. Eftersom molekylerna också rör sig snabbare ökar kollisioner mellan enzymer och substrat också. Således ju lägre kinetisk energi, desto lägre temperatur i systemet och, på samma sätt, desto högre kinetisk energi, desto större är temperaturen i systemet.
När temperaturen i systemet ökar kommer molekylernas inre energi i systemet att öka., Molekylernas inre energi kan innefatta molekylernas translationsenergi, vibrationsenergi och rotationsenergi, den energi som är involverad i molekylernas kemiska bindning samt den energi som är involverad i icke-motsvarande interaktioner. En del av denna värme kan omvandlas till kemisk potentiell energi. Om denna kemiska potentiella energiökning är tillräckligt stor kan några av de svaga bindningarna som bestämmer den tredimensionella formen hos de aktiva proteinerna brytas. Detta kan leda till termisk denaturering av proteinet och därmed inaktivera proteinet., Således kan för mycket värme orsaka hastigheten av en enzymkatalyserad reaktion att minska eftersom enzymet eller substratet blir denaturerad och inaktiv.
optimal temperatur
varje enzym har ett temperaturområde där en maximal reaktionshastighet uppnås. Detta maximala kallas temperaturen optimalt för enzymet. Den optimala temperaturen för de flesta enzymer är ca 98,6 grader Fahrenheit (37 grader Celsius). Det finns också enzymer som fungerar bra vid lägre och högre temperaturer., Till exempel har arktiska djur enzymer anpassade till lägre optimala temperaturer; djur i ökenklimat har enzymer anpassade till högre temperaturer. Men enzymer är fortfarande proteiner, och som alla proteiner börjar de bryta ner vid temperaturer över 104 grader Fahrenheit. Därför bestäms intervallet av enzymaktivitet av den temperatur vid vilken enzymet börjar aktiveras och temperaturen vid vilken proteinet börjar sönderdelas.,
relaterade tjänster
enzymkinetik
Enzymologiska analyser
för att diskutera mer service detaljer, kontakta oss genom att ringa 1-631-562-8517, eller e-posta oss på [email protected].
















Lämna ett svar