når temperaturen øker, så gjør frekvensen av enzymet reaksjoner. En ti grader celsius økning i temperaturen vil øke aktiviteten av de fleste enzymer med 50% til 100%. Variasjoner i reaksjon temperatur så liten som 1 eller 2 grader kan innføre endringer av 10% til 20% i resultatene. Denne økningen er bare opp til et visst punkt før forhøyet temperatur bryter strukturen av enzymet. Når enzymet er denaturert, det kan ikke bli reparert., Som hvert enzym er forskjellige i sin struktur og båndene mellom aminosyrer og peptider, temperaturen for denaturing er spesifikke for hvert enzym. Fordi de fleste dyr enzymer raskt bli denaturert ved temperaturer over 40°C, mest enzym bestemmelser er utført noe under det temperatur.
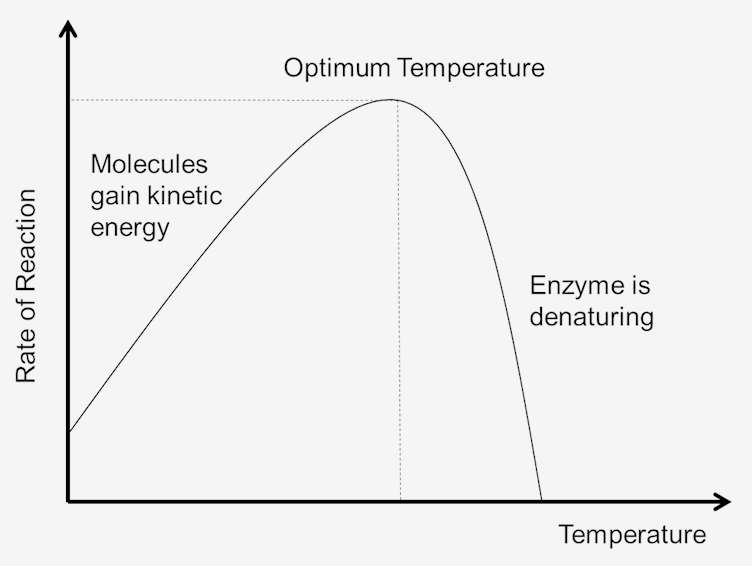 Figur 1. Effekt av temperatur på reaksjon pris.
Figur 1. Effekt av temperatur på reaksjon pris.
Over en periode av tid, enzymer vil være deaktivert, selv ved moderate temperaturer. Lagring av enzymer på 5°C eller lavere er vanligvis den mest passende. Lavere temperaturer føre til tregere kjemiske reaksjoner., Enzymer vil til slutt bli inaktive ved minusgrader, men vil gjenopprette de fleste av deres enzymaktivitet når temperaturen øker igjen, mens noen enzymer miste sin aktivitet når frosset.
Kinetisk Energi og Indre Energi
temperaturen på et system som til en viss grad er et mål for den kinetiske energien til molekylene i systemet. Kollisjoner mellom alle molekylene øker når temperaturen øker. Dette skyldes økning i hastighet og kinetisk energi som følger temperaturen øker. Med raskere hastigheter, vil det bli mindre tid mellom kollisjoner., Dette resulterer i mer molekyler nå aktivering energi, noe som øker frekvensen av reaksjoner. Siden molekylene er også går fortere, kollisjoner mellom enzymer og underlag også øke. Dermed lavere den kinetiske energien, jo lavere temperatur i systemet, og motsatt, jo høyere er den kinetiske energien, jo større temperaturen i systemet.
Som temperaturen i systemet er økt, den indre energien til molekylene i systemet vil øke., Den indre energien til molekylene kan omfatte translasjonsforskning energi, vibrerende energi og rotasjonsenergi av molekyler, energi som er involvert i kjemiske bånd av molekyler samt energi som er involvert i nonbonding interaksjoner. Noe av denne varmen kan bli omdannet til kjemisk potensiell energi. Hvis dette kjemisk potensiell energi økningen er stor nok noen av de svake båndene som avgjør tre-dimensjonal form av aktive proteiner kan være ødelagt. Dette kan føre til termisk denaturering av proteiner og dermed inactivate protein., Dermed for mye varme kan føre til prisen av et enzym-catalyzed reaksjon for å redusere fordi enzymet eller underlaget blir denaturert og inaktive.
Optimal Temperatur
Hvert enzym har et temperaturområde som har en maksimal hastighet på reaksjonen er oppnådd. Dette maksimum er kjent som optimal temperatur av enzymet. Den optimale temperaturen for de fleste enzymer er om den 98,6 grader Fahrenheit (37 grader Celsius). Det er også enzymer som fungerer bra på lavere og høyere temperaturer., For eksempel, Arktiske dyr har enzymer som er tilpasset lavere optimal temperatur; dyr i ørkenen klima har enzymer som er tilpasset høyere temperaturer. Imidlertid, enzymer er fortsatt proteiner, og som alle proteiner, de begynner å bryte ned ved temperaturer over 104 grader Fahrenheit. Derfor utvalg av enzymaktivitet er bestemt av temperaturen som enzym begynner å aktivere og den temperaturen som protein begynner å brytes ned.,
Relaterte Tjenester
enzymkinetikk
Enzymology Analyser
for Å diskutere mer detaljer i tjenesten, kan du kontakte oss ved å ringe 1-631-562-8517, eller e-post til oss på [email protected].
















Legg igjen en kommentar