ein patient mit…
Torsade de pointes
Torsades de Pointes
Eva Buller Viqueiraa, Juana Cabello Pulidob und María José Ibáñez, Bulpec
Adresse für die Korrespondenz
abstract
wir präsentieren den Fall eines Mannes behandelt Anfällen mit diazepam bei mehreren Gelegenheiten. Schließlich wird ein erworbenes Long-QT-Syndrom gezeigt, das ihn für Torsades de Pointes prädisponiert, die sich mit Anfällen manifestieren und daher fälschlicherweise behandelt werden., Das Long-QT-Syndrom wird überprüft und beschreibt die verschiedenen angeborenen und erworbenen Ursachen, die elektrokardiographische Diagnose und die korrigierte Messung des QT-Intervalls entsprechend der Herzfrequenz und der Behandlung.
Schlüsselwörter: Torsades de Pointes. Verlängerte QT-Syndrom. Herzrhythmusstörungen.
ZUSAMMENFASSUNG
Die Gegenwart ist der Fall eines Mannes, der mehrmals wegen Anfällen mit Diazepam behandelt wurde. Schließlich wurde ein erworbenes Long-QT-Syndrom nachgewiesen, das ihn für Torsades de pointes prädisponierte, sich als Anfälle manifestierte und fortan fälschlicherweise behandelt wurde., Das Long-QT-Syndrom wird überprüft und beschreibt die verschiedenen Ursachen des langen QT-Intervalls, sowohl angeboren als auch erworben, elektrokardiographische Diagnose, nach Herzfrequenz und Behandlung.
Schlüsselwörter: Torsades de Pointes. Langes QT-Syndrom. Arrhythmien, Herz.
Einleitung
Das Long-QT-Syndrom (SQTL) ist eine Veränderung, die durch eine Verlängerung der Repolarisation des ventrikulären Aktionspotentials verursacht wird und für maligne Torsades de Pointes (TdP) – Arrhythmien oder ventrikuläre Tachykardie prädisponiert, die zu Kammerflimmern führen können., Es kann angeboren oder erworben sein, verursacht durch Medikamente, hydroelektrolytische Veränderungen, Fasten oder verschiedene Pathologien. 1957 beschrieben Jervell und Lange-Nielsen den ersten Fall von familiärer SQTL mit Taubheit. Selzer und Wray beschrieben erstmals 1964 QT-Verlängerung und Kammerflimmern. Im Jahr 1966 beschrieb Dessertenne TdP1, 2.
klinischer Fall
Wir präsentieren den Fall eines 36-jährigen Mannes, Ex-Drogenabhängigen, der sich derzeit in Methadonbehandlung befindet, Raucher und chronischer Enolismus., Sie ist in Behandlung mit Cyproteron, leidet an Angst-depressive Störung in der Behandlung mit Fluoxetin 20 mg, Dikalium Clorazepat 50 mg und Alprazolam 2 mg.diagnostiziert mit hepatitis-C-virus-Infektion und hamartoma.
der Patient wurde bei Verdacht auf tonisch-klonische Anfälle in Krankenhausnotfälle überwiesen. Die zweite Krise wurde beobachtet und trat in einen Atemstillstand ein, der nach der Beatmung mit Ambú nachgab. Der Patient berichtete, in den zwei Tagen vor dem Vorfall keinen Alkohol genommen zu haben. Phenytoin, Pantoprazol und intravenöses (iv) Diazepam wurden verabreicht., Bei der Ankunft in der Notaufnahme des Krankenhauses war er asymptomatisch und mit ständiger körperlicher Untersuchung ohne irgendetwas von Interesse. Neben anderen ergänzenden Tests wurden Blutbild mit einem hohen mittleren korpuskulären Volumen( VCM), Biochemie mit Hypokaliämie, Hypokalzämie und Hypertransaminasämie (GOT und GPT) angefordert, die alle in wahrscheinlicher Beziehung zu ihrem chronischen Enolismus standen. Myoglobin war ebenfalls erhöht und im Zusammenhang mit Anfällen; positiv für Methadon und Benzodiazepine (bzd), Rest uninteressant. Auf dem Elektrokardiogramm (EKG) wurde ein mit Bigeminismus kompatibles Bild aufgezeichnet., Ihm wurden CLK iv, Pantoprazol iv, Propranolol oral, intramuskuläres Thiaminhydrolorid (im), Pyridoxinhydrochlorid iv verabreicht und eine elektrokardiographische Überwachung durchgeführt. Die Biochemie wurde wiederholt, wobei Hypokaliämie, Gesamt-CK, CK-Mb und MB erhöht blieben.
Er wurde für die Innere Medizin zugelassen und die Biochemie wurde erneut wiederholt, ohne Kalium einzubeziehen. Hielt VCM, GOT, GGT und CK Summen hoch. Das EKG wurde normalisiert und der patient blieb asymptomatisch., Er wurde mit chronischem Enolismus, Makrozytose, Rhythmusstörung durch Hypoxie diagnostiziert, ohne auszuschließen, dass es durch BZD und Krampfanfälle durch enolische Deprivation war. Er wurde unter Beibehaltung seiner üblichen Behandlung entlassen.
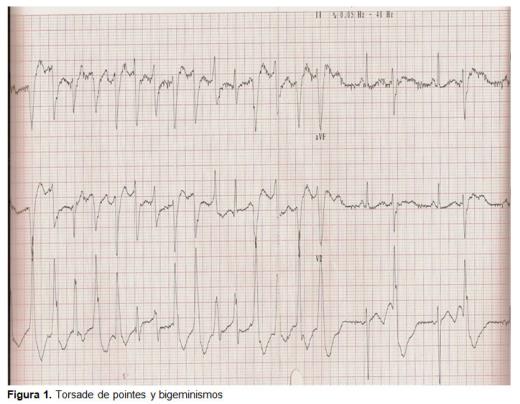
im folgenden Monat wurde er für einen kurzlebigen Anfall und spontane Genesung zurückgebracht. Er kam asymptomatisch in der Notaufnahme an, mit einem ungestörten Scan, erhöhter VCM, Hypokaliämie und dem EKG mit isolierten ventrikulären Extrasystolen. Er wurde entlassen., Am nächsten Tag wurde er erneut von seinem Gesundheitszentrum für tonisch-klonische Anfälle ohne enolische Deprivation überwiesen. Es wurde unter Beobachtung gehalten und mit Diazepam iv und kontinuierlicher elektrokardiographischer Aufzeichnung behandelt. Der Fall wurde mit dem diensthabenden Kardiologen besprochen, der die Aufzeichnung mit folgenden Befunden bewertete: ventrikulärer Bigeminismus mit Verlängerung des QT-Intervalls (0, 52 SEK.); ventrikulärer Bigeminismus und PDT (Abbildung 1); ventrikuläre Tachykardie. Es wurde mit CLK iv, Magnesiumsulfat iv und elektrokardiographischer Überwachung behandelt., Während der Aufnahme wurde die elektrokardiographische Kontrolle verbessert, zeigte ein QT-Intervall von 0,44 Sek., abgeflachte T-Wellen und U-Wellen (Zeichen von Hypokaliämie), bis zur Normalisierung bei der Entladung mit einem Sinusrhythmus bei 50 Schlägen pro Minute (lpm), keine Anzeichen von Blockade, keine Anzeichen von Hohlraumwachstum, mit elektrischer Achse innerhalb der Grenzen der normalen, keine Anzeichen von Ischämie, das QT-Intervall von 0,4 sek., normalisierte T-Wellen und keine Anwesenheit von U-Welle (Abbildung 2)., Das klinische Urteil bei der Entlassung war eine Synkope aufgrund einer ventrikulären Tachykardie vom Typ PDT aufgrund einer langen QT, die sekundär aufgrund einer Hypokaliämie aufgrund von chronischem Alkoholismus und mangelnder Einnahme erworben wurde. Es erforderte keine spezifische Behandlung bei der Entlassung oder Nachsorge, da die Ursache erworben und beseitigt wurde.

Das lange QT-Syndrom kann sowohl durch angeborene als auch durch erworbene Faktoren verursacht werden., Angeborene werden durch genetische Veränderungen verursacht, die die Proteine der Natrium-oder Kalium-Transmembrankanäle kodieren. Infolgedessen erhöht sich die positive Ladung in der Zelle aufgrund eines Mangels an Natriumabgabe oder einer Erhöhung des Kaliumeinsatzes. Es verlängert die ventrikuläre Repolarisation und verlängert daher das QT-Intervall, prädisponiert für PDT. Die Prävalenz beträgt 1/2000, wobei die Synkope die erste häufigste klinische Manifestation ist. Symptomatische Patienten beginnen etwa 12 Jahre alt in 50% der Fälle und bei 40 in 90 %., Es ist eine der Ursachen für plötzlichen Kindstod; 10 % dieser Todesfälle haben eine genetische Mutation, die SQTL verursacht. Zahlreiche Arten von angeborenen SQTL wurden identifiziert (Romano-Ward-Syndrom Subtypen von QTL1-QTL15 und Jervell-Syndrom und Lange-Nielson-Subtypen JLN1-JLN2), aber die häufigsten sind diejenigen, die in Romano-Ward-Syndrom, und unter ihnen QTL1-3., Es gibt Faktoren, die für kardiale Ereignisse entsprechend den verschiedenen Arten von QTL prädisponieren; Zum Beispiel wird QTL-1 durch körperliche Aktivität oder emotionalen Stress (Schwimmen), im Fall von QTL-2 durch auditive Reize (wie einen Wecker oder eine Glocke), postpartalen oder emotionalen Stress stimuliert. Kürzlich wurde beobachtet, dass Epilepsie bei Typ 2 um 39% häufiger auftritt. Die Differentialdiagnose ist wichtig, da viele fälschlicherweise als Epilepsie aufgrund von Anfällen behandelt werden, die während der PDT auftreten., Die Diagnose der angeborenen SQTL basiert auf dem Schwartz-Score (Tabelle 1), der elektrokardiographische Befunde, klinische und Familienanamnese auswertet. Angeborene SQTL wird mit einer Summe von 3,5 oder mehr und ohne erworbene Ursachen diagnostiziert. Es gibt Fälle von Werten von 1 bis 3, in denen die QT-Verlängerung latent ist,sie kann jedoch durch Durchführung einer Holter-oder elektrokardiographischen Reihe während körperlicher Betätigung oder eines Adrenalintests entlarvt werden3, 4.,Arzneimittelwechselwirkung, lange Fastenperioden oder Proteinflüssigkeitsdiäten, Enzyminhibitoren (Grapefruitsaftaufnahme), Sinusbradykardie oder Brüche aufgrund von Sinusblockade oder atrioventrikulärem Block, Leber-oder Nierenversagen, strukturelle Herzkrankheit (ischämische Herzkrankheit, Herzinsuffizienz, ventrikuläre Hypertrophie), weibliches Geschlecht (bei längerem QT-Intervall physiologische Zustände), fortgeschrittenes Alter, Vorhofflimmern Kardioversion und akuter Schlaganfall.5,
um ein SQTL zu diagnostizieren, müssen wir zuerst wissen, wie das QT-Intervall im EKG korrekt gemessen wird. Das QT-Intervall umfasst vom Beginn des QRS-Komplexes bis zum Beginn der T-Welle und sollte dort gemessen werden, wo die Q-Welle visualisiert werden kann (normalerweise in DII, V5 oder V6). Die QT-Messung muss an die Herzfrequenz angepasst werden; Dies wird korrigiertes QT (QTc) genannt und wird nach der Bazett-Formel berechnet.
QTc= QT / √RR
Das RR-Intervall ist der Abstand zwischen der R-Welle und der nächsten R-Welle., Beide Werte müssen in Millimetern (mm) gemessen und in Sekunden übergeben werden, bevor sie in die Formel eingegeben werden. Das mm wird gemessen und mit 0,04 multipliziert. Bei Arrhythmie sollten mehrere Messungen durchgeführt und der Mittelwert berechnet werden. Wir müssen besonders darauf achten, die U-Welle nicht in die T-Welle aufzunehmen. falls das Ende der T-Welle nicht gut differenziert werden kann, ist es ratsam, die Tangensenmethode zu verwenden, die darin besteht, zu berücksichtigen, dass die T-Welle am Schnittpunkt der Tangente des am meisten geneigten Abschnitts des T-Wellenabkömmlings und der Grundlinie endet (Abbildung 3)., Normalwerte des QT-Intervalls werden zwischen unter 12 Jahren und über 12 Jahren unterschieden. Bei Personen über 12 Jahren wird der Unterschied zwischen Männern und Frauen als normal zwischen 0,39 und 0,45 bei ersteren und zwischen 0,39 und 0,46 bei letzteren angesehen.3

eine Verlängerung des QT-Intervalls kann zu bereiten Tipp torsion oder TdP. Das TdP ist eine unregelmäßige polymorphe Variation des QRS, die sich von positiv zu negativ ändert, um wieder von vorne zu beginnen; Es scheint, dass die Spitzen um die elektrische Achse gedreht sind., Die Herzfrequenz liegt zwischen 150 und 300 BPM mit unregelmäßigen RR-Intervallen. Es beginnt plötzlich und wird nicht aufrechterhalten.
Die Behandlung von PDT ist Kardioversion im Falle eines hämodynamischen Kompromisses. Alle Medikamente, die eine QT-Dehnung verursachen können, sollten zurückgezogen werden. Magnesiumsulfat ist entweder angeboren oder erworben und unabhängig vom Magnesiumspiegel im Serum die erste Wahl: Ein Bolus von 2 g in 2-3 Minuten, gefolgt von einer iv-Infusion von 2-4 mg/min, und ein zweiter Bolus kann passieren, wenn die TdP wiederholt wird, während die iv-Infusion verabreicht wird., Es unterstützt Schwangerschaft. Es kann Bluthochdruck und Asystolie produzieren. Das Gegenmittel für Magnesiumsulfat ist Calciumgluconat. Isoproterenol wird verwendet, wenn Magnesiumsulfat und Schrittmacher versagen oder geschultes Personal nicht geschult ist, um den Schrittmacher zu platzieren. Es sollte nicht bei angeborenen SQTL verwendet werden. Als Nebenwirkungen sind häufig Herzklopfen, Gesichtsrötung und Hitze. Was die Serumkaliumspiegel anbelangt, so hat sich gezeigt, dass es vorzuziehen ist, dass sie sich in den hohen Grenzen des Normalwerts befinden und möglicherweise eine iv-Verabreichung erfordern., Es ist in der Schwangerschaft nicht kontraindiziert und sollte niemals Bolus verabreicht werden, da es zu Arrhythmien und Herzdepressionen führen kann, die zum Tod führen. Es sollte mit EKG überwacht werden. Der intravenöse temporäre Schrittmacher kann bei etwa 100 BPM platziert werden, wenn Magnesium PDT nicht verhindert.
Eine Langzeitbehandlung von SQTL bei Erwerb ist nicht erforderlich, da sie nach Beseitigung der Ursache normalerweise nachgibt. Auf der anderen Seite, wenn es angeboren ist, ist es ratsam, orale β-Blocker zu verwenden, indem man von einem 0.97 zu einem 0.31 kardiale Ereignisse pro Patient und Jahr verringert., Es ist ratsam, während des Trainings eine Herzfrequenz unter 130 BPM aufrechtzuerhalten. Kaliumpräparate werden in QTL-2 empfohlen. Implantierbarer Defibrillator und sympathische Denervation des linken Herzens werden bei Patienten mit Herzstillstand in der Vorgeschichte empfohlen, klinisch vor dem Lebensjahr oder JLN-1. Bildung ist wichtig, um auslösende Reize zu vermeiden (körperliche Bewegung, Schwimmen, Schlafmangel, Hörreize, intensive sympathische Reize, Schmerzen, Leiden, Wut erschreckend)3,6-8.,
Es scheint uns, dass die QTc-Messung in der Grundversorgung etwas übersehen wird, obwohl sie einfach zu berechnen und sehr zugänglich ist, da das EKG ein sehr häufiger ergänzender Test in unserer täglichen Arbeit ist. Es einfach zu erkennen und darauf einzuwirken, kann schwerwiegende Folgen haben. Eine systematische Messung des QT-Intervalls zur Früherkennung bei der Behandlung mit Medikamenten, die es verlängern, kann wie bei Elektrolytveränderungen ratsam sein.
Interessenkonflikt
die Autoren erklären, dass sie keinen Interessenkonflikt haben.,
Bibliographie
1. Kallergis EM, Goudis CA, Simantirakis EN, KOCHIADAKIS GE, Vardas PE. Mechanismen, Risikofaktoren und Management des erworbenen Long-QT-Syndroms: eine umfassende Überprüfung. Wissenschaftliches Weltjournal. 2012; 2012: 212178.
3. Muñoz Castellano J. Langes QT-Syndrom und Torsade de Pointes. Notfall. 2004; 16: 85-92.
















Schreibe einen Kommentar