Når temperaturen stiger, gør det også hastigheden af en .ymreaktioner. En ti graders stigning i temperatur vil øge aktiviteten af de fleste en .ymer med 50% til 100%. Variationer i reaktionstemperatur så små som 1 eller 2 grader kan indføre ændringer på 10% til 20% i resultaterne. Denne stigning er kun op til et bestemt punkt, indtil den forhøjede temperatur bryder en .ymets struktur. Når en .ymet er denatureret, kan det ikke repareres., Da hvert en .ym er forskelligt i dets struktur og bindinger mellem aminosyrer og peptider, er temperaturen for denaturering specifik for hvert en .ym. Da de fleste dyreen .ymer hurtigt denatureres ved temperaturer over 40.C, udføres de fleste en .ymbestemmelser noget under denne temperatur.
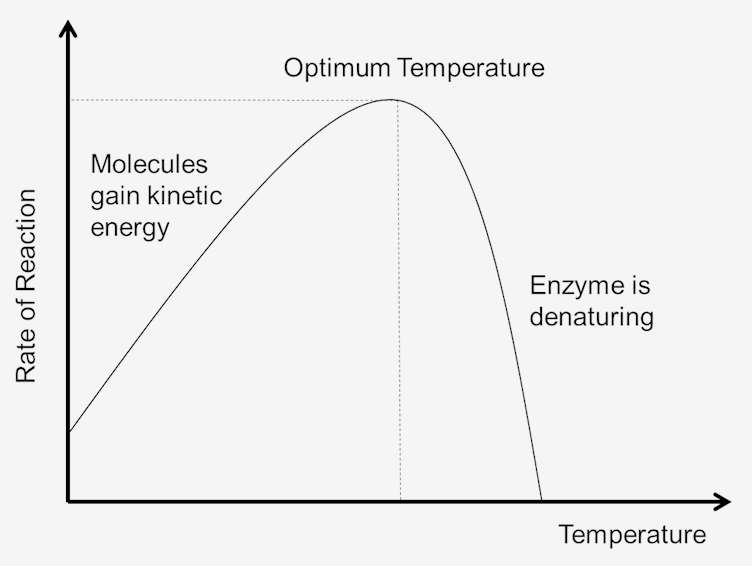 Figur 1. Effekt af temperatur på reaktionshastigheden.
Figur 1. Effekt af temperatur på reaktionshastigheden.
Over en periode deaktiveres en .ymer ved lige moderate temperaturer. Opbevaring af en .ymer ved 5 C C eller derunder er generelt den mest egnede. Lavere temperaturer fører til langsommere kemiske reaktioner., En .ymer vil til sidst blive inaktive ved frysetemperaturer, men vil genoprette det meste af deres en .ymaktivitet, når temperaturerne stiger igen, mens nogle en .ymer mister deres aktivitet, når de fryses.
kinetisk energi og intern energi
temperaturen i et system er til en vis grad et mål for den kinetiske energi af molekylerne i systemet. Kollisioner mellem alle molekyler stiger, når temperaturen stiger. Dette skyldes stigningen i hastighed og kinetisk energi, der følger temperaturstigninger. Med hurtigere hastigheder vil der være mindre tid mellem kollisioner., Dette resulterer i, at flere molekyler når aktiveringsenergien, hvilket øger reaktionshastigheden. Da molekylerne også bevæger sig hurtigere, øges også kollisioner mellem en .ymer og underlag. Således jo lavere kinetisk energi, jo lavere temperatur af systemet og ligeledes, jo højere kinetisk energi, jo større temperatur af systemet.
Når temperaturen i systemet øges, vil den indre energi af molekylerne i systemet stige., Den indre energi af molekylerne kan omfatte translationel energi, vibrationelle energi og roterende energi af molekylerne, den energi, der er involveret i kemiske binding af de molekyler, samt den energi, der er involveret i nonbonding interaktioner. Noget af denne varme kan omdannes til kemisk potentiel energi. Hvis denne kemiske potentielle energiforøgelse er stor nok, kan nogle af de svage bindinger, der bestemmer den tredimensionelle form af de aktive proteiner, blive brudt. Dette kan føre til termisk denaturering af proteinet og således inaktivere proteinet., Således kan for meget varme forårsage, at hastigheden af en en .ymkatalyseret reaktion falder, fordi en .ymet eller substratet bliver denatureret og inaktivt.
optimal temperatur
Hvert en .ym har et temperaturområde, hvor en maksimal reaktionshastighed opnås. Dette maksimum er kendt som en .ymets temperaturoptimum. Den optimale temperatur for de fleste en .ymer er omkring 98,6 grader Fahrenheit (37 grader Celsius). Der er også en .ymer, der fungerer godt ved lavere og højere temperaturer., For eksempel har arktiske dyr en .ymer tilpasset til lavere optimale temperaturer; dyr i ørkenklimaer har en .ymer tilpasset højere temperaturer. En .ymer er dog stadig proteiner, og som alle proteiner begynder de at bryde ned ved temperaturer over 104 grader Fahrenheit. Derfor bestemmes rækkevidden af en .ymaktivitet af den temperatur, ved hvilken en .ymet begynder at aktiveres, og den temperatur, ved hvilken proteinet begynder at nedbrydes.,
Relaterede Tjenester
enzymkinetik
Enzymologi Analyser
for At diskutere flere detaljer, kan du kontakte os ved at ringe 1-631-562-8517, eller e-mail til os på [email protected].
















Skriv et svar