W tym momencie stężenie kwasu i jego jonów jest równe. W takim przypadku anulują wyrażenie rodzaju.
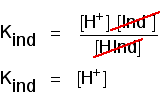
możesz użyć tego, aby dowiedzieć się, jakie jest pH w tym połowie drogi., Jeśli przestawisz Ostatnie równanie tak, aby stężenie jonów wodorowych znajdowało się po lewej stronie, a następnie przekonwertujesz na pH i pKind, otrzymasz:
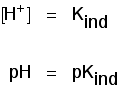
oznacza to, że punkt końcowy wskaźnika zależy całkowicie od jego wartości pKind. Dla wskaźników, które przyjrzeliśmy się powyżej, są to:
| wskaźnik | pKind |
|---|---|
| lakmus | 6.5 |
| methyl orange | 3.7 |
| fenoloftaleina | 9.,3 |
zakres pH wskaźników
wskaźniki nie zmieniają Ostro koloru przy jednym określonym pH (podanym przez ich pKind). Zamiast tego zmieniają się w wąskim zakresie pH.
Załóżmy, że równowaga jest mocno na jednej stronie, ale teraz dodajesz coś, aby zacząć ją przesuwać. Gdy równowaga się przesunie, zaczniesz uzyskiwać coraz więcej drugiego koloru, a w pewnym momencie oko zacznie go wykrywać.
Załóżmy na przykład, że w roztworze alkalicznym był pomarańczowy metylowy, więc dominującym kolorem był żółty., Teraz zacznij dodawać kwas, aby równowaga zaczęła się przesuwać.
w pewnym momencie pojawi się wystarczająco dużo czerwonej formy pomarańczy metylowej, aby roztwór zaczął przybierać pomarańczowy odcień. W miarę dodawania większej ilości kwasu czerwony w końcu stanie się tak dominujący, że nie widać żółtego.
następuje stopniowa, płynna zmiana z jednego koloru na drugi, zachodząca w zakresie pH. zgodnie z szorstką „zasadą kciuka”, widoczna zmiana odbywa się około 1 jednostki pH po obu stronach wartości pKind.,
dokładne wartości dla trzech wskaźników, które przyjrzeliśmy się to:
| wskaźnik | pKind | zakres pH |
|---|---|---|
| lakmus | 6.5 | 5 – 8 |
| methyl orange | 3.7 | 3.1 – 4.4 |
| fenoloftaleina | 9.3 | 8.3 – 10.0 |
zmiana koloru lakmusu następuje po niezwykle szeroki zakres, ale jest przydatny do wykrywania kwasów i zasad w laboratorium, ponieważ zmienia kolor wokół pH 7., Pomarańcza metylowa lub fenoloftaleina byłyby mniej przydatne.
jest to łatwiej widoczne diagramowo.
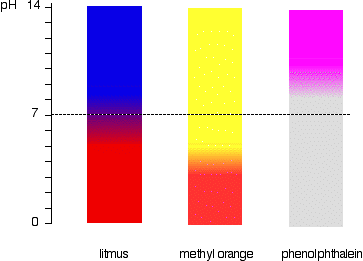
na przykład pomarańczowy metylowy byłby żółty w dowolnym roztworze o pH większym niż 4,4. Nie mógł odróżnić słabego kwasu o pH 5 lub silnej Zasady o pH 14.
wybór wskaźników miareczkowania
pamiętaj, że punkt równoważności miareczkowania jest miejscem, w którym zmieszano dwie substancje dokładnie w proporcjach równania., Oczywiście należy wybrać wskaźnik, który zmienia kolor jak najbliżej tego punktu równoważności. To zmienia się w zależności od miareczkowania.
mocny kwas v mocna podstawa
następny wykres pokazuje krzywą pH dodawania mocnego kwasu do mocnej zasady. Nakłada się na nią zakresy pH pomarańczy metylowej i fenoloftaleiny.
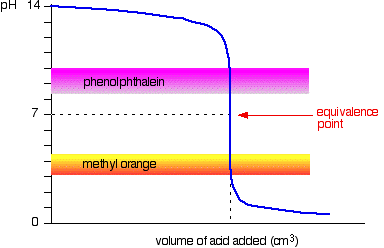
widać, że żaden wskaźnik nie zmienia koloru w punkcie równoważności.,
jednak wykres jest tak stromy w tym momencie, że nie będzie praktycznie żadnej różnicy w objętości dodawanego kwasu, niezależnie od wybranego wskaźnika. Jednak przy każdym wskaźniku sensownym byłoby miareczkowanie do możliwie najlepszego koloru.
Jeśli używasz fenoloftaleiny, będziesz miareczkować, aż po prostu stanie się bezbarwna (przy pH 8,3), ponieważ jest to tak blisko, jak można dostać się do punktu równoważności.
z drugiej strony, stosując pomarańczę metylową, można miareczkować, aż w roztworze pojawi się pierwszy ślad pomarańczy., Jeśli rozwiązanie stanie się czerwone, oddalamy się od punktu równoważności.
mocny kwas v słaba zasada
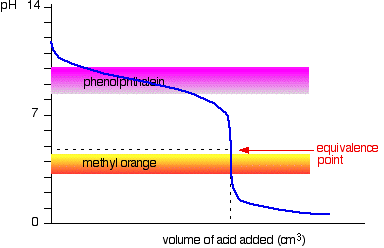
tym razem jest oczywiste, że fenoloftaleina będzie całkowicie bezużyteczna. Jednak pomarańcza metylowa zaczyna zmieniać się z żółtej w pomarańczową bardzo blisko punktu równoważności.
musisz wybrać wskaźnik, który zmienia kolor na stromym fragmencie krzywej.
słaby kwas v mocna baza
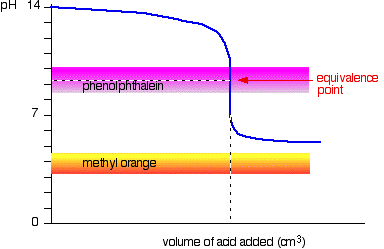
tym razem pomarańcza metylowa jest beznadziejna!, Jednak fenoloftaleina zmienia kolor dokładnie tam, gdzie chcesz.
słaby kwas v słaba zasada
krzywa dotyczy przypadku, gdy kwas i zasada są równie słabe – na przykład kwas etanowy i roztwór amoniaku. W innych przypadkach punkt równoważności będzie przy innym pH.
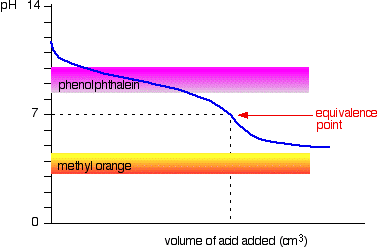
widać, że żaden wskaźnik nie jest użyteczny. Fenoloftaleina skończy się zmieniać na długo przed punktem równoważności, a pomarańcza metylowa całkowicie odpada z wykresu.,
Możliwe jest znalezienie wskaźnika, który zaczyna się zmieniać lub kończy się w punkcie równoważności, ale ponieważ pH punktu równoważności będzie różne w zależności od przypadku, nie można uogólnić.
ogólnie rzecz biorąc, nigdy nie miareczkujesz słabego kwasu i słabej zasady w obecności wskaźnika.
roztwór węglanu sodu i rozcieńczony kwas solny
jest to interesujący przypadek szczególny., Jeśli używasz fenoloftaleiny lub pomarańczy metylowej, oba dadzą prawidłowy wynik miareczkowania – ale wartość z fenoloftaleiną będzie dokładnie o połowę mniejsza od pomarańczowej metylowej.
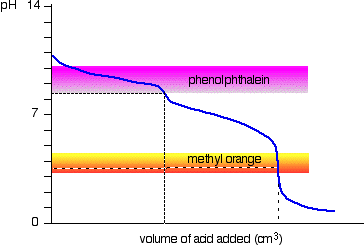
tak się składa, że fenoloftaleina zakończyła swoją zmianę koloru dokładnie w pH punktu równoważności pierwszej połowy reakcji, w której wytwarzany jest wodorowęglan sodu.
![]()
![]()
pomarańcz metylowa zmienia barwę dokładnie w pH punktu równoważności drugiego etapu reakcji.,
![]()
![]()
pytania, aby sprawdzić swoje zrozumienie
Jeśli jest to pierwszy zestaw pytań, które zrobiłeś, przeczytaj stronę wprowadzającą przed rozpoczęciem. Musisz użyć przycisku Wstecz w przeglądarce, aby wrócić tutaj później.
pytania dotyczące wskaźników
odpowiedzi
gdzie chciałbyś teraz pojechać?
do menu równowagi kwasowo-zasadowej . . .
do menu Chemia Fizyczna . . .
do Menu Głównego . . .,
















Dodaj komentarz