un paziente con…
Torsade de pointes
Torsades de Pointes
Eva Buller Viqueiraa, Juana Cabello Pulidob e María José Ibáñez Bulpec
indirizzo per corrispondenza
abstract
presentiamo il caso di un maschio trattato per convulsioni con diazepam in diverse occasioni. Infine, viene dimostrata una sindrome acquisita del QT lungo che lo predisponeva a torsioni di punta che si manifestavano con convulsioni e, quindi, trattate erroneamente., La sindrome del QT lungo viene rivista, descrivendo le diverse cause sia congenite che acquisite, la diagnosi elettrocardiografica, la misurazione corretta dell’intervallo QT in base alla frequenza cardiaca e al trattamento.
parole chiave: Torsades de Pointes. Sindrome QT prolungata. aritmia.
ABSTRACT
Il presente è il caso di un uomo trattato in diverse occasioni per convulsioni con diazepam. Alla fine, è stata dimostrata una sindrome acquisita del QT lungo che lo ha predisposto a torsades de pointes, manifestandosi come convulsioni e d’ora in poi trattati erroneamente., La sindrome del QT lungo viene rivista, descrivendo le diverse cause dell’intervallo QT lungo, sia congenite che acquisite, diagnosi elettrocardiografica, in base alla frequenza cardiaca e al trattamento.
Parole chiave: Torsades de Pointes. Sindrome del QT lungo. Aritmie, cardiache.
introduzione
La sindrome del QT lungo (SQTL) è un’alterazione causata da un allungamento della ripolarizzazione del potenziale d’azione ventricolare e predispone ad aritmie maligne di torsione di punta (TdP) o tachicardia ventricolare che possono portare alla fibrillazione ventricolare., Può essere congenito o acquisito causato da farmaci, alterazioni idroelettrolitiche, digiuno o varie patologie. Nel 1957 Jervell e Lange-Nielsen descrissero il primo caso di SQTL familiare con sordità. Selzer e Wray descrissero per la prima volta il prolungamento del QT e la fibrillazione ventricolare nel 1964. Nel 1966 Dessertenne descrisse TdP1, 2.
caso clinico
presentiamo il caso di un uomo di 36 anni, ex tossicodipendente attualmente in trattamento con metadone, fumatore e con enolismo cronico., È transessuale nel trattamento con ciproterone, soffre di disturbo ansioso-depressivo nel trattamento con fluoxetina 20 mg, clorazepato dipotassico 50 mg e alprazolam 2 mg.diagnosticato con infezione da virus dell’epatite C e amartoma.
il paziente è stato indirizzato alle emergenze ospedaliere per sospetto di crisi tonico-cloniche. La seconda crisi è stata testimoniata, entrando arresto respiratorio che ha dato modo dopo la ventilazione con ambú. Il paziente ha riferito di non aver assunto alcol nei due giorni precedenti l’incidente. Sono stati somministrati fenitoina, pantoprazolo e diazepam per via endovenosa (iv)., All’arrivo al pronto soccorso dell’ospedale era asintomatico e con costante esame fisico senza nulla di interessante. Tra gli altri test complementari sono stati richiesti emocromo ad alto volume corpuscolare medio( VCM), biochimica con ipopotassiemia, ipocalcemia e ipertransaminasemia (GOT e GPT), il tutto in probabile relazione al loro enolismo cronico. Anche la mioglobina era elevata e correlata alle convulsioni; positivo per metadone e benzodiazepine (bzd), resto poco interessante. Sull’elettrocardiogramma (ECG) è stata registrata un’immagine compatibile con il bigeminismo., È stato somministrato CLK iv, pantoprazolo iv, propranololo per via orale, idroluro di tiamina intramuscolare (im), piridossina cloridrato iv ed è stato eseguito il monitoraggio elettrocardiografico. La biochimica è stata ripetuta, mantenendo ipokaliemia, CK totale, CK-Mb e MB elevati.
è stato ammesso responsabile della Medicina Interna e la biochimica è stata ripetuta di nuovo senza includere il potassio. Mantenuto VCM, OTTENUTO, GGT e CK totali alti. L’ECG è stato normalizzato e il paziente è rimasto asintomatico., Gli è stato diagnosticato un enolismo cronico, macrocitosi, disturbo del ritmo da ipossia senza escludere che fosse da BZD e convulsioni da deprivazione enolica. È stato dimesso mantenendo il suo solito trattamento.
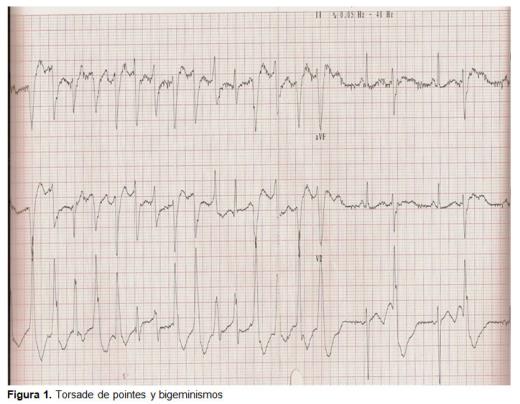
il mese successivo è stato riportato per un attacco di breve durata e un recupero spontaneo. Arrivò al pronto soccorso asintomatico, con una scansione indisturbata, VCM elevata, ipopotassiemia e l’ECG presentava extrasistoli ventricolari isolati. E ‘ stato dimesso., Il giorno dopo è stato di nuovo indirizzato dal suo centro di salute per convulsioni tonico-cloniche senza privazione enolica. È stato tenuto sotto osservazione e trattato con diazepam iv e registrazione elettrocardiografica continua. Il caso è stato discusso con il cardiologo di turno, che ha valutato il record con i seguenti risultati: bigeminismo ventricolare con prolungamento dell’intervallo QT (0,52 SEC.); bigeminismo ventricolare e PDT (Figura 1); tachicardia ventricolare. È stato trattato con CLK iv, solfato di magnesio iv e monitoraggio elettrocardiografico., Durante il ricovero, la elettrocardiografici di controllo è stato migliorato, ha presentato un intervallo QT di 0,44 sec., appiattite le onde T e U onde (segno di ipokaliemia), fino a normalizzazione allo scarico con un ritmo sinusale a 50 battiti al minuto (lpm), senza segni di ostruzione, senza segni di cavità di crescita, con asse elettrico entro i limiti di normale, senza segni di ischemia, l’intervallo QT di 0.4 sec., normalizzato onde T e n presenza di U onda (Figura 2)., Il giudizio clinico alla dimissione era sincope a causa di tachicardia ventricolare tipo PDT a causa di QT lungo acquisito secondariamente a ipopotassiemia a causa di alcolismo cronico e mancanza di assunzione. Non ha richiesto un trattamento specifico alla dimissione o al follow-up poiché la causa è stata acquisita ed eliminata.

discussione
La sindrome del QT lungo può essere causata da fattori congeniti e acquisiti., I congeniti sono causati da alterazioni genetiche che codificano le proteine dei canali transmembrana del sodio o del potassio. Di conseguenza, la carica positiva all’interno della cellula aumenta a causa della mancanza di uscita di sodio o di un aumento dell’apporto di potassio. Prolunga la ripolarizzazione ventricolare e quindi allunga l’intervallo QT, predisponendo alla PDT. La prevalenza è 1/2000, con la sincope che è la prima manifestazione clinica più comune. I pazienti sintomatici iniziano a circa 12 anni nel 50% dei casi e a 40 nel 90%., È una delle cause della morte infantile improvvisa; il 10% di queste morti ha una mutazione genetica che causa SQTL. Sono stati identificati numerosi tipi di SQTL congeniti (sottotipi della sindrome di Romano-Ward di QTL1-QTL15 e sindrome di jervell e sottotipi di Lange-Nielson JLN1-JLN2), ma i più comuni sono quelli inclusi nella sindrome di Romano-Ward, e tra questi QTL1-3., Ci sono fattori che predispongono agli eventi cardiaci secondo i diversi tipi di QTL; ad esempio, QTL-1 è stimolato da attività fisica o stress emotivo (nuoto), nel caso di QTL-2 da stimoli uditivi (come una sveglia o una campana), postpartum o stress emotivo. Recentemente è stato osservato che l’epilessia è più comune tra il tipo 2, del 39 %. La diagnosi differenziale è importante perché molti sono erroneamente trattati come epilessia a causa di convulsioni che si verificano durante la PDT., La diagnosi di SQTL congenito si basa sul punteggio di Schwartz (Tabella 1), che valuta i risultati elettrocardiografici, la storia clinica e familiare. SQTL congenito viene diagnosticato con una somma di 3,5 o più e senza cause acquisite. Ci sono casi di punteggi da 1 a 3 in cui il prolungamento del QT è latente, ma può essere smascherato eseguendo una serie Holter o elettrocardiografica durante l’esercizio fisico o il test dell’epinefrina3,4.,interazione farmacologica, lunghi periodi di digiuno o diete proteiche liquide, inibitori enzimatici (assunzione di succo di pompelmo), bradicardia sinusale o rotture dovute a blocco seno-atriale o atrioventricolare, insufficienza epatica o renale, cardiopatia strutturale (cardiopatia ischemica, insufficienza cardiaca, ipertrofia ventricolare), sesso femminile (per avere un intervallo QT più lungo condizioni fisiologiche), età avanzata, fibrillazione atriale cardioversione e ictus acuto.5,
per diagnosticare un SQTL, dobbiamo prima sapere come misurare correttamente l’intervallo QT sull’ECG. L’intervallo QT comprende dall’inizio del complesso QRS all’inizio dell’onda T e deve essere misurato dove l’onda Q può essere visualizzata (normalmente in DII, V5 o V6). La misurazione del QT deve essere regolata sulla frequenza cardiaca; questo è chiamato QT corretto (QTc) e viene calcolato utilizzando la formula di Bazett.
QTc = QT / √RR
l’intervallo RR è la distanza tra l’onda R e l’onda R successiva., Entrambi i valori devono essere misurati in millimetri (mm) e passati a secondi prima di inserirli nella formula. Il mm viene misurato e moltiplicato per 0,04. In caso di aritmia devono essere effettuate diverse misurazioni e viene calcolata la media. Dobbiamo prestare particolare attenzione a non includere l’onda U nell’onda T. nel caso di non riuscire a differenziare bene la fine dell’onda T è consigliabile utilizzare il metodo tangente, che consiste nel considerare che l’onda T termina all’intersezione della tangente della porzione più inclinata della discendente dell’onda T e della linea di base (figura 3)., I valori normali dell’intervallo QT si distinguono tra meno di 12 anni e oltre 12 anni. In quelli di età superiore ai 12 anni, la differenza tra maschi e femmine è considerata normale tra 0,39 e 0,45 nel primo e tra 0,39 e 0,46 nel secondo.3

il prolungamento dell’intervallo QT può predisporre alla torsione della punta o al TdP. Il TdP è una variazione polimorfica irregolare del QRS che cambia da positivo a negativo per ricominciare; sembra che le punte siano attorcigliate attorno all’asse elettrico., La frequenza cardiaca è compresa tra 150 e 300 BPM con intervalli RR irregolari. Inizia improvvisamente e non è sostenuto.
il trattamento della PDT è cardioversione in caso di compromesso emodinamico. Tutti i farmaci che possono causare l’allungamento del QT devono essere ritirati. Il solfato di magnesio è di prima scelta sia congenito che acquisito e indipendente dal livello di magnesio nel siero: un bolo di 2 g da passare in 2-3 minuti seguito da infusione endovenosa 2-4 mg/min e un secondo bolo può passare se il TdP viene ripetuto durante l’infusione endovenosa., Supporta la gravidanza. Può produrre alta pressione sanguigna e asistolia. L’antidoto per il solfato di magnesio è il gluconato di calcio. L’isoproterenolo viene utilizzato quando il solfato di magnesio e il pacemaker falliscono o il personale addestrato non è addestrato a posizionare il pacemaker. Non dovrebbe essere usato in SQTL congenito. Come effetti collaterali sono palpitazioni comuni, arrossamento del viso e calore. Per quanto riguarda i livelli sierici di potassio, è stato dimostrato che è preferibile che siano nei limiti elevati del normale e che possano richiedere la sua somministrazione endovenosa., Non è controindicato in gravidanza e non dovrebbe mai essere somministrato in bolo perché può produrre aritmie e depressione cardiaca che portano alla morte. Dovrebbe essere monitorato con ECG. Il pacemaker temporaneo per via endovenosa può essere posizionato a circa 100 BPM se il magnesio non riesce a prevenire la PDT.
il trattamento a lungo termine di SQTL in caso di acquisizione non è necessario, perché una volta eliminata la causa di solito cede il passo. D’altra parte, se è congenito è consigliabile utilizzare β-bloccanti orali diminuendo da 0,97 a 0,31 eventi cardiaci per paziente e anno., Si consiglia di mantenere una frequenza cardiaca durante l’esercizio al di sotto di 130 BPM. Gli integratori di potassio sono raccomandati in QTL-2. Il defibrillatore impiantabile e la denervazione simpatica cardiaca sinistra sono raccomandati in pazienti con una storia di arresto cardiaco, clinica prima dell’anno di vita o JLN-1. L’educazione è importante per evitare stimoli precipitanti (esercizio fisico, nuoto, mancanza di sonno, stimoli uditivi, stimoli simpatici intensi, dolore, sofferenza, rabbia sorprendente)3,6-8.,
ci sembra che la misurazione del QTc sia qualcosa di trascurato nelle cure primarie nonostante sia facile da calcolare e molto accessibile, poiché l’ECG è un test complementare molto comune nel nostro lavoro quotidiano. Semplicemente riconoscerlo e agire su di esso può prevenire gravi conseguenze. La misurazione sistematica dell’intervallo QT per la sua diagnosi precoce nel trattamento con farmaci che lo allungano può essere consigliabile, come nelle alterazioni elettrolitiche.
conflitto di interessi
gli autori dichiarano di non avere alcun conflitto di interessi.,
bibliografia
1. Kallergis EM, Goudis CA, Simantirakis EN, KOCHIADAKIS GE, Vardas PE. Meccanismi, fattori di rischio e gestione della sindrome del QT lungo acquisito: una revisione completa. Rivista scientifica mondiale. 2012; 2012: 212178.
3. Muñoz Castellano J. Sindrome del QT lungo e Torsione di punta. Emergenza. 2004; 16: 85-92.
















Lascia un commento