un patient…
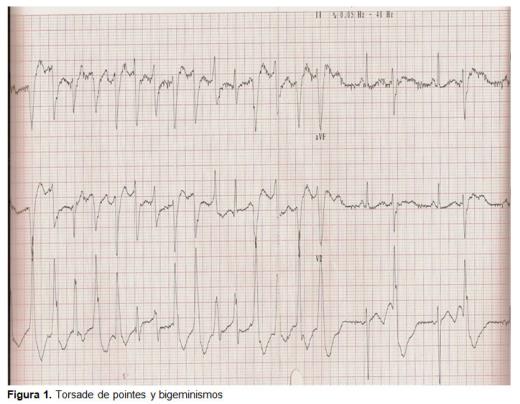
Torsade de pointes
torsades de Pointes
Eva Buller Viqueiraa, Juana Cabello Pulidob et María José Ibáñez Bulpec
adresse pour la correspondance
résumé
Nous présentons le cas d’un homme traité pour des convulsions au diazépam à plusieurs reprises. Enfin, un syndrome du QT long acquis est démontré qui le prédisposait aux torsades de pointes se manifestant par des convulsions et, par conséquent, traité à tort., Le syndrome du QT long est examiné, décrivant les différentes causes congénitales et acquises, le diagnostic électrocardiographique, la mesure corrigée de l’intervalle QT en fonction de la fréquence cardiaque et du traitement.
mots clés: Torsades de Pointes. Syndrome QT prolongé. Des Arythmies Cardiaques.
résumé
Le présent est le cas d’un homme traité à plusieurs reprises pour des convulsions au diazépam. Finalement, un syndrome du QT long acquis a été démontré qui le prédisposait à des torsades de pointes, se manifestant par des crises et désormais traitées par erreur., Le syndrome du QT long est examiné, décrivant les différentes causes du long intervalle QT, à la fois congénital et acquis, diagnostic électrocardiographique, en fonction de la fréquence cardiaque et du traitement.
mots clés: Torsades de Pointes. Le Syndrome du QT Long. Arythmies, Cardiaques.
introduction
le syndrome du QT Long (SQTL) est une altération causée par un allongement de la repolarisation du potentiel d’action ventriculaire et prédispose aux arythmies malignes des torsades de pointes (TdP) ou à la tachycardie ventriculaire pouvant entraîner une fibrillation ventriculaire., Il peut être congénital ou acquis causé par des médicaments, des altérations hydroélectrolytiques, le jeûne ou diverses pathologies. En 1957, Jervell et Lange-Nielsen ont décrit le premier cas de SQTL familial avec surdité. Selzer et Wray ont décrit pour la première fois l’allongement de L’intervalle QT et la fibrillation ventriculaire en 1964. En 1966 Dessertenne décrit TdP1, 2.
cas clinique
Nous présentons le cas d’un homme de 36 ans, ex-toxicomane actuellement sous traitement à la méthadone, fumeur et atteint d’énolisme chronique., Elle est transsexuelle en traitement à la cyprotérone, souffre de trouble anxieux-dépressif en traitement à la fluoxétine 20 mg, Au clorazépate dipotassique 50 mg et à l’alprazolam 2 mg.diagnostiqué avec une infection par le virus de l’hépatite C et un hamartome.
le patient a été dirigé vers les urgences hospitalières en raison de soupçons de crises tonico-cloniques. La deuxième crise a été témoin, entrant arrêt respiratoire qui a cédé après ventilation avec ambú. Le patient a déclaré ne pas avoir pris d’alcool dans les deux jours précédant l’incident. La phénytoïne, le pantoprazole et le diazépam par voie intraveineuse (iv) ont été administrés., À son arrivée au service des urgences de l’hôpital, il était asymptomatique et soumis à un examen physique constant sans rien d’intéressant. Entre autres tests complémentaires ont été demandés une numération formule sanguine avec un volume corpusculaire moyen élevé( VCM), une biochimie avec hypokaliémie, hypocalcémie et hypertransaminasémie (GOT et GPT), tous en relation probable avec leur énolisme chronique. La myoglobine était également élevée et liée aux convulsions; positive pour la méthadone et les benzodiazépines (bzd), reste sans intérêt. Sur l’électrocardiogramme (ECG), une image compatible avec le bigéminisme a été enregistrée., On lui a administré du CLK iv, du pantoprazole iv, du propranolol par voie orale, de l’hydrolorure de thiamine (im) intramusculaire, du chlorhydrate de pyridoxine iv et une surveillance électrocardiographique a été effectuée. La biochimie a été répétée, maintenant l’hypokaliémie, la CK totale, la CK-Mb et la MB élevées.
Il a été admis en charge de la médecine interne et de la biochimie répétée sans inclure de potassium. Maintenu VCM, GOT, GGT et CK totaux élevés. L’ECG a été normalisé et le patient est resté asymptomatique., On lui a diagnostiqué une énolisme chronique, une macrocytose, un trouble du rythme par hypoxie sans exclure que ce soit par BZD et des convulsions par privation énolique. Il a été libéré tout en maintenant son traitement habituel.
le mois suivant, il a été ramené pour une crise de courte durée et un rétablissement spontané. Il est arrivé à l’urgence asymptomatique, avec un scanner non perturbé, une VCM élevée, une hypokaliémie et L’ECG ont présenté des extrasystoles ventriculaires isolées. Il a été libéré., Le lendemain, il a été renvoyé de son centre de santé pour des crises tonico-cloniques sans privation énolique. Il a été maintenu en observation et traité avec du diazépam iv et un enregistrement électrocardiographique continu. Le cas a été discuté avec le cardiologue de garde, qui a évalué le dossier avec les résultats suivants: bigéminisme ventriculaire avec allongement de l’intervalle QT (0,52 sec.); bigéminisme ventriculaire et PDT (Figure 1); tachycardie ventriculaire. Il a été traité avec CLK iv, sulfate de magnésium iv et surveillance électrocardiographique., Lors de l’admission, le contrôle électrocardiographique a été amélioré, présenté un intervalle QT de 0,44 s, des ondes t aplaties et des ondes U (signe d’hypokaliémie), jusqu’à la normalisation à la décharge avec un rythme sinusal à 50 battements par minute (lpm), aucun signe de blocage, aucun signe de croissance de la cavité, avec axe électrique dans les limites de la normale, aucun signe d’ischémie, l’intervalle QT de 0,4 s, des ondes t normalisées et aucune présence d’onde U (Figure 2)., Le jugement clinique à la sortie était une syncope due à une tachycardie ventriculaire de type PDT due à un QT Long acquis secondairement à une hypokaliémie due à l’alcoolisme chronique et au manque d’apport. Il n’a pas nécessité de traitement spécifique à la sortie ou de suivi puisque la cause a été acquise et éliminée.

discussion
QT Long, syndrome peut être causé par deux congénitales et acquises facteurs., Congénitales sont causées par des altérations génétiques qui codent les protéines des canaux transmembranaires de sodium ou de potassium. En conséquence, la charge positive à l’intérieur de la cellule augmente, en raison d’un manque de sodium, de sortie ou d’une augmentation de potassium d’entrée. Il prolonge la repolarisation ventriculaire et allonge donc l’intervalle QT, prédisposant à la PDT. La prévalence est de 1/2000, la syncope étant la première manifestation clinique la plus courante. Les patients symptomatiques commencent à environ 12 ans dans 50% des cas et à 40 ans dans 90% des cas., C’est l’une des causes de la mort subite du nourrisson; 10% de ces décès ont une mutation génétique causant SQTL. De nombreux types de SQTL congénitaux ont été identifiés (sous-types du syndrome de Romano-Ward de QTL1-QTL15 et du syndrome de jervell et sous-types de Lange-Nielson JLN1-JLN2), mais les plus courants sont ceux inclus dans le syndrome de Romano-Ward, et parmi eux QTL1-3., Il existe des facteurs qui prédisposent aux événements cardiaques selon les différents types de QTL; par exemple, QTL-1 est stimulé par une activité physique ou un stress émotionnel (natation), dans le cas de QTL-2 par des stimuli auditifs (tels qu’un réveil ou une cloche), un stress post-partum ou émotionnel. Récemment, il a été observé que l’épilepsie est plus fréquente chez le Type 2, de 39 %. Le diagnostic différentiel est important car beaucoup sont traités à tort comme de l’épilepsie en raison de crises qui se produisent pendant la TDP., Le diagnostic de sqtl congénital est basé sur le score de Schwartz (Tableau 1), qui évalue les résultats électrocardiographiques, les antécédents cliniques et familiaux. Sqtl congénital est diagnostiqué avec une somme de 3,5 ou plus et sans causes acquises. Il existe des cas de scores de 1 à 3 dans lesquels l’allongement de L’intervalle QT est latent, mais il peut être démasqué en effectuant une série Holter ou électrocardiographique pendant un exercice physique ou un test d’épinéphrine3,4.,interaction médicamenteuse, longues périodes de jeûne ou de régimes protéiques liquides, inhibiteurs enzymatiques (consommation de jus de pamplemousse), bradycardie sinusale ou pauses dues à un bloc sino-auriculaire ou auriculo-ventriculaire, insuffisance hépatique ou rénale, cardiopathie structurelle (cardiopathie ischémique, insuffisance cardiaque, hypertrophie ventriculaire), sexe féminin (pour avoir un intervalle QT plus long conditions physiologiques), âge avancé, fibrillation auriculaire cardioversion et accident vasculaire cérébral aigu.5,
pour diagnostiquer un SQTL, il faut d’abord savoir mesurer correctement l’intervalle QT sur L’ECG. L’intervalle QT comprend du début du complexe QRS au début de l’onde T, et doit être mesuré là où L’onde Q Peut être visualisée (normalement en DII, V5 ou V6). La mesure du QT doit être ajustée à la fréquence cardiaque; c’est ce QU’on appelle le QT corrigé (QTc) et est calculé à l’aide de la formule de Bazett.
QTc= QT / √RR
l’intervalle RR est la distance entre l’onde R et la prochaine vague de R., Les deux valeurs doivent être mesurées en millimètres (mm) et passées en secondes avant de Les entrer dans la formule. Le mm est mesuré et multiplié par 0,04. En cas d’arythmie, plusieurs mesures doivent être prises et la moyenne est calculée. Nous devons accorder une attention particulière à ne pas inclure L’onde U dans l’onde T. en cas de ne pas pouvoir bien différencier l’extrémité de l’onde T il est conseillé d’utiliser la méthode tangente, qui consiste à considérer que l’onde T se termine à l’intersection de la tangente de la partie la plus inclinée de l’onde T descendante et de la ligne de base (figure 3)., Les valeurs normales de l’intervalle QT sont distinguées entre moins de 12 ans et plus de 12 ans. Chez les plus de 12 ans, la différence entre les hommes et les femmes est considérée comme normale entre 0,39 et 0,45 chez les premiers et entre 0,39 et 0,46 chez les seconds.3

allongement de l’intervalle QT peut prédisposer à la pointe de torsion ou de TdP. Le TdP est une variation polymorphe irrégulière du QRS qui passe du positif au négatif pour recommencer; il semble que les pointes soient tordues autour de l’axe électrique., La fréquence cardiaque est comprise entre 150 et 300 BPM avec des intervalles RR irréguliers. Il commence soudainement et n’est pas soutenu.
le traitement de la TDP est la cardioversion en cas de compromis hémodynamique. Tous les médicaments pouvant provoquer un allongement de L’QT doivent être retirés. Le sulfate de magnésium est de premier choix congénital ou acquis et indépendant du taux de magnésium dans le sérum: un bolus de 2 g à passer en 2-3 minutes suivi d’une perfusion iv 2-4 mg/min et un second bolus peut passer si le TdP est répété pendant la perfusion iv., Il prend en charge la grossesse. Il peut produire une pression artérielle élevée et une asystolie. L’antidote pour le sulfate de magnésium est le gluconate de calcium. L’isoprotérénol est utilisé lorsque le sulfate de magnésium et le stimulateur cardiaque échouent ou que le personnel qualifié n’est pas formé pour placer le stimulateur cardiaque. Il ne doit pas être utilisé dans le SQTL congénital. Comme les effets secondaires sont des palpitations courantes, des rougeurs du visage et de la chaleur. En ce qui concerne les taux de potassium sérique, il a été démontré qu’il est préférable qu’ils soient dans les limites élevées de la normale et qu’ils puissent nécessiter son administration iv., Il n’est pas contre-indiqué pendant la grossesse et ne doit jamais être administré en bolus car il peut produire des arythmies et une dépression cardiaque entraînant la mort. Il doit être surveillé avec ECG. Le stimulateur cardiaque temporaire intraveineux peut être placé à environ 100 BPM si le magnésium ne prévient pas la TDP.
le traitement à long terme de SQTL en cas d’acquisition n’est pas nécessaire, car une fois la cause éliminée, elle cède généralement. D’autre part, s’il est congénital, il est conseillé d’utiliser des β-bloquants oraux en diminuant de 0,97 à 0,31 événements cardiaques par patient et par an., Il est conseillé de maintenir une fréquence cardiaque pendant l’exercice en dessous de 130 BPM. Les suppléments de Potassium sont recommandés dans QTL-2. Le défibrillateur Implantable et la dénervation sympathique cardiaque gauche sont recommandés chez les patients ayant des antécédents d’arrêt cardiaque, cliniques avant l’année de vie ou JLN-1. L’éducation est importante pour éviter de déclencher des stimuli (exercice physique, natation, manque de sommeil, stimuli auditifs, stimuli sympathiques intenses, douleur, souffrance, colère surprenante)3,6-8.,
Il nous semble que la mesure QTc est quelque chose de négligé dans les soins primaires bien qu’elle soit facile à calculer et très accessible, car L’ECG est un test complémentaire très courant dans notre travail quotidien. Le simple fait de le reconnaître et d’agir dessus peut prévenir de graves conséquences. La mesure systématique de l’intervalle QT pour sa détection précoce dans le traitement avec des médicaments qui l’allongent peut être recommandée, comme dans les altérations électrolytiques.
conflit d’intérêt
les auteurs déclarent n’avoir aucun conflit d’intérêt.,
bibliographie
1. Kallergis EM, Goudis CA, Simantirakis FR, KOCHIADAKIS GE, Vardas PE. Mécanismes, facteurs de risque et gestion du Syndrome du QT long acquis: un examen complet. Revue Scientifique Mondiale. 2012; 2012: 212178.
3. Muñoz Castellano J. syndrome du QT Long et Torsade de Pointes. Urgence. 2004; 16: 85-92.
















Laisser un commentaire