D Kelly1, G Crotty1, J O’Mullane2, M Stapleton2, B Sweeney1, SS O’Sullivan1
Oddělení 1Neurology a 2Biochemistry, Cork University Hospital, Wilton, Korek
Abstrakt
prvním krokem při zjišťování potenciální Wilson onemocnění je sérového ceruloplazminu testování, přičemž úroveň nižší než 0,2 g/L je sugestivní onemocnění., Naším cílem bylo zjistit, jaký podíl irské populace měl nízkou hladinu ceruloplazminu, zda byla vhodně sledována nízká měření a jaké byly klinické výsledky. Od srpna 2003 do října 2009 jsme provedli retrospektivní revizi všech měření sérového ceruloplazminu ve velkém terciárním referenčním centru v jižním Irsku. Klinické údaje, sérový ceruloplasmin, testy jaterních funkcí, zprávy o biopsii mědi a jater byly zaznamenány tam, kde jsou k dispozici. 1573 pacientů mělo během 7letého studovaného období měření ceruloplazminu v séru. 96 pacientů (6.,1%) mělo hladinu ceruloplazminu < 0, 2 g/L a z těchto pouze 3 pacientů mělo Wilsonovu chorobu. Byla pouze 1 nová diagnóza. Pouze 27 pacientů (28, 1%) mělo nějakou formu potvrzujícího testování. Podle zkušeností našeho centra je pozitivní prediktivní hodnota významně nízké hladiny ceruloplazminu 11,1% (95% CI 2,91-30,3%). V praxi není měření ceruloplazminu s nízkým sérem často následováno vhodným potvrzujícím testováním., Měření sérového ceruloplazminu jako jedinečného diagnostického testu na Wilsonovu chorobu nebo jako součást baterie nevybraných testů jaterního screeningu je nevhodné a nízké výtěžnosti.
Úvod
Wilsonova choroba (WD) je vzácné autosomálně recesivní vada v hepatocelulární doprava mědi nacházejí v 3 100 000 lidmi1. To může vést k chronickému ukládání mědi v játrech, mozku a dalších tkáních, což má za následek hepatotoxicitu a neuropsychiatrické následky2., Americká Asociace pro Studium Jaterních Nemocí (AASLD) doporučuje screening pro WD v každém jednotlivém ve věku od 3 do 55 let s jaterní abnormality nejisté příčiny, zejména ty s komorbidní nevysvětlené neurologické disorders3. Prvním krokem při zjišťování potenciální WD je sérového ceruloplazminu měření, přibližně 85 až 90 procent pacientů s WD mít nízká hladina ceruloplazminu glukózy4., Nízký ceruloplasmin však není specifický pro WD; může být důsledkem malabsorpce, jiných onemocnění jater, enteropatie ztrácejících bílkoviny, získaného nedostatku mědi a dědičné aceruloplasminemie5. Ceruloplasmin je také reaktant akutní fáze a může být zvýšen v zánětlivých stavech včetně pacientů s WD s aktivní hepatitidou6. Hyper-estrogenní stavy včetně těhotenství nebo užívání perorální antikoncepční pilulky mohou také zvýšit hladiny ceruloplazminu, protože ceruloplasmin mRNA má estrogen reagující proti proudu pro jeho transkripci7. Hladiny ceruloplazminu menší než 0.,2g/L bylo prokázáno, že v jedné studii, že mají citlivost přes 98%, specificita více než 55% a pozitivní prediktivní hodnotu přes 48% pro diagnostiku WD na genotyp-ověřené patients8.
Nicméně, další výzkum naznačuje pozitivní prediktivní hodnoty ceruloplazminu <0,2 g/L, pokud se používá samotný u pacientů s dysfunkcí jater může být tak nízké, jak je 5.9%1. Z tohoto důvodu pokyny doporučují řadu potvrzujících testů včetně vyšetření štěrbinovou lampou pro detekci kroužků Kayser-Fleischer (KF) a odhadu 24hodinové močové mědi.3., Pro osoby s neurčitými výsledky,včetně jaterní biopsie, mohou být vyžadována další vyšetření k určení koncentrace jaterní mědi nebo molekulárního testování mutací ATP7B9, 10. Evropská Asociace pro Studium Jater (EASL) pokyny klinické praxe také uznává omezení sérového ceruloplazminu měření jednoho testu, a doporučuje použití kombinace testů, které odrážejí ‚narušen metabolismu mědi s diagnostický systém bodování na základě jejich výsledky11., Naše studie hodnotila výskyt nízkých hladin ceruloplazminu v populaci a klinické indikace pro testování. Zjistili jsme, zda bylo provedeno další diagnostické testování a jaký byl klinický význam těchto výsledků.
Metody
provedli Jsme retrospektivní přehled všech ceruloplazminu měření v Cork University Hospital, klinické laboratoře, která slouží velké sítě primární péče, specializované kliniky, a 800-postel terciární neurologické a hepatological referral centre v období od srpna 2003 do října 2009., Časové období bylo vybráno tak, aby zahrnovalo maximální dostupné údaje. Studii schválila Etická komise nemocnice. Klinické údaje, sérový ceruloplasmin, testy jaterních funkcí, zprávy o biopsii mědi a jater byly zaznamenány tam, kde jsou k dispozici. Nefelometrie byla technika používaná referenční laboratoří pro měření sérového ceruloplazminu během studovaného období. Hodnoty ceruloplazminu menší než 0,2 g / L jsme považovali za potenciálně pozitivní pro WD v souladu s publikovanými pokyny. 3., Diagnóza WD byla stanovena na základě výsledků potvrzujících testů (moč a jaterní měď, oftalmologické vyšetření) a dokumentace lékařských záznamů. Výsledky genetického testování byly zaznamenány tam, kde jsou k dispozici. WD heterozygoty byly definovány jako ty, které mají pouze jednu mutaci způsobující onemocnění, pokud neexistují jiné podpůrné rysy. Data byla analyzována pomocí SPSS verze 21.
Výsledky
Demografie testované populace
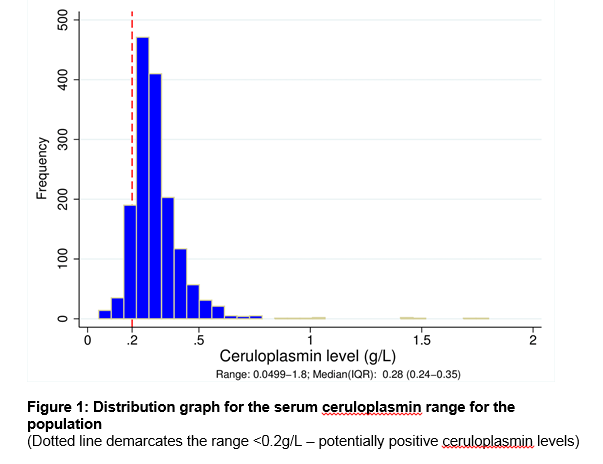
Naše laboratoř v Cork city, Irsko slouží jako nadregionální centrum pro celkový počet obyvatel 1,1 milionu lidí., V laboratorní databázi bylo 1573 pacientů, kteří měli v průběhu 7letého studovaného období měření ceruloplasminu v séru. Tabulka 1 popisuje demografické údaje a zdroj doporučení podle klinické specializace. U pacientů mladších 3 let nebo více než 55 let bylo objednáno celkem 476 hladin ceruloplazminu v séru (30, 3%), což je skupina mimo doporučení AASLD3. Viz Obrázek 1 pro rozsah hladin ceruloplazminu v celé populaci. Medián ceruloplazminu úrovni bylo 0.28 g/L (5. percentil = 0.18, 95 percentil = 0,5 g/L)., Tam byl významný rozdíl ve střední úrovni pro muže a ženy na 0,27 g/L a 0,3 g/L, respektive (p<0.05). Mezi věkem a hladinou ceruloplazminu byla slabá pozitivní korelace s nižším věkem spojeným s nižší hladinou ceruloplazminu, r =.124, n = 1573, p <.0005.
Tabulka 1:
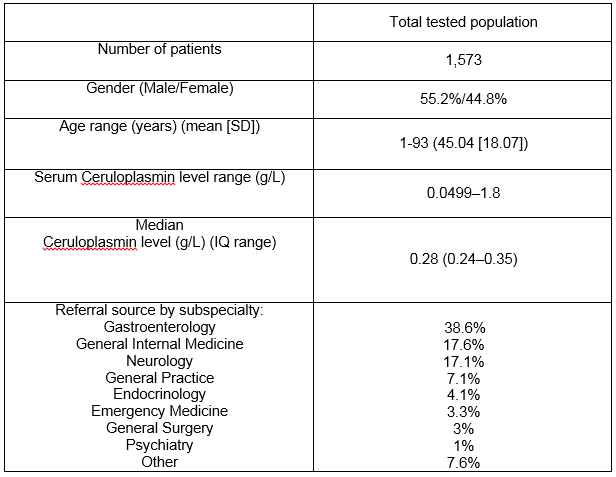
Pozitivní ceruloplazminu výsledky
96 pacientů (muži:ženy = 72%:28%) z celé kohorty (6.1%) měl ceruloplazminu úrovni <0.,2 g / L (viz Obrázek 1). Nejčastější indikace pro testování byla přítomnost abnormality jaterních testů (61.5%), poruchy pohybu (o 18,8%) a psychiatrické poruchy (7.3%). 40,6% skupiny byly následně uvedeny konečné onemocnění jater diagnóza, z nichž nejčastější byl alkoholické onemocnění jater (o 14,6%), následuje tukové non alkoholické jaterní onemocnění (8.3%). Pouze 3 z 96 pacientů (3, 1%) mělo WD. Dva z těchto pacientů byli dříve diagnostikováni a byli znovu testováni na sledování onemocnění. Jeden pacient byl nově diagnostikován s WD během studovaného období., Jeho zvýšené 24hodinové vylučování mědi močí, Kayser-Fleisher kroužky spolu s nízkou hladinou ceruloplazminu v séru potvrdily diagnózu. Všechny 3 WD pacienti měli ceruloplazminu < 0.05 g/L. kromě toho, 1 jedinec projevující se třesem byl identifikován jako WD dopravce s jediným ATP7B mutace. Jeho genetická analýza nebyla v souladu se složeným heterozygotem a nikdy nevyvinul žádné další klinické příznaky.
potvrzující testování Wilsonovy choroby
po pozitivním / sugestivním výsledku ceruloplazminu 27/96 pacientů (28.,1%) měla nějakou formu potvrzujícího testování WD. 14 pacientů (14, 5%) bylo oftalmologicky vyšetřeno na kroužky Kayser-Fleisher. 10 pacientů (10, 4%) mělo jaterní biopsii pro kvantifikaci jaterní mědi. 23 pacientů (24%) mělo kvantifikaci mědi v moči. Průměrný follow-up období od okamžiku prvního testování byl 51,4 měsíců (SD 30.3 měsíců). Subspecialita non-neurology / gastroenterologie byla významně méně pravděpodobná při následných vyšetřeních. (p<0.01). Pouze 4 z 27 pacientů (14.,8%), kteří měli další testování, byli v péči subspecialit non-neurology / gastroenterologie.
Ceruloplazminu jako screeningový diagnostický test,
Diskuse
Měření z ceruloplazminu je často výzva v hodnocení a řízení pacientů s elevaci jaterních enzymů. V našem přehledu 7 let vzorců objednávání ceruloplazminu jsme zjistili špatné dodržování pokynů AASLD. Významná část testované populace byla mimo věkové rozmezí doporučené AASLD. Je velmi neobvyklé, že se Wilsonova choroba vyskytuje po věku 4012 let., Ve velké retrospektivní přezkum hladiny ceruloplazminu v 5023 pacientů, počet potřebný k testu pro pozdní nástup Wilson onemocnění (>40 let věku), aby výsledek v 1 nová diagnóza byla 284713. V mnoha případech nebyly abnormality jater nejisté etiologie a častější nemoci ještě nebyly vyloučeny. Několik z těch, s nízké hladiny ceruloplazminu měl chronickou hepatitidou nebo alkoholem indukované nemoci jater – stavy spojené s falešně pozitivní výsledky sekundární špatné jaterní syntetické function1., Méně než 30% populace studie mělo vhodné následné vyšetření pozitivního výsledku ceruloplazminu, jako je oční vyšetření na kroužky KF nebo jaterní biopsie pro barvení mědi. Měření ceruloplazminu byla požadována různými subspeciality, nejčastějšími jsou gastroenterologie, neurologie a internisté. Nejčastějším důvodem testování bylo hodnocení zvýšení jaterních enzymů nebo zjištění onemocnění jater. Lékaři, kteří nebyli gastroenterologové nebo neurologové, měli menší pravděpodobnost, že provedou potvrzující vyšetření (p<0.01)., To naznačuje nedostatek obeznámenosti s jinými subspecialitami s diagnostickým algoritmem vyšetřování nezbytným k potvrzení nebo vyloučení WD.
měření sérového ceruloplazminu s mezní hladinou menší než 0, 2 g/L mělo v naší studii nízkou PPV pro WD podobnou dříve publikované práci1. To se týká nízké pravděpodobnosti pre-testu diagnózy u neselektované populace s vysokou prevalencí onemocnění jater se známou etiologií. Snížení referenčního rozsahu na 0,14 by zlepšilo výkon testu bez nepříznivého vlivu na citlivost., Větší diagnostická přesnost s tímto nižším prahem byla hlášena v předchozích studiích s upozorněním na místní ověření nutné8. V této studii, sérového ceruloplazminu koncentrace nižší než 0,20, 0.14, a 0.10 g/L vykazovaly pozitivní prediktivní hodnoty 48,3%, 100% a 100%, respektive, Ve validační skupině, sérového ceruloplazminu práh 0,14 g/L vykreslen 100% citlivost a specifičnost. Je však možné, že ne každý pacient s WD byl zachycen na základě tohoto screeningového testu., Jak již bylo zmíněno, mohou existovat falešně negativní výsledky pro WD tváří v tvář infekci nebo zánětu14. Těhotenství a doplňková estrogenová terapie mohou mít podobný dopad15. Budoucí požadavky/interpretace testů by měly brát v úvahu takové zmírňující klinické faktory. Způsob testování může ovlivnit výsledky. Sérového ceruloplazminu mohou být měřeny enzymaticky jeho mědi závislé monoaminooxidázy činnost na specifické substráty nebo protilátky závislé testy. Ta zahrnuje nefelometrii, radioimunoanalýzu a radiální imunodifuzi., Výsledky jsou obecně podobné, až na protilátce závislé a immunodiffusion testy, které mohou přeceňovat ceruloplazminu v krvi. Nadhodnocení může dojít, protože obě testovací metody nerozlišují mezi apoceruloplasmin (ceruloplazminu není vázáno na měď) a holoceruloplasmin (ceruloplasmin s jeho plným 6 atomy mědi v molekule)16. Nefelometrie byla technika používaná důsledně během našeho studijního období.
tato studie měla několik omezení. Nesledovali jsme pacienty, kteří měli normální (> 0.,2G / L) hladiny ceruloplazminu v séru, aby se zajistilo, že se následně nevyvinuly WD. Takže jsme možná nezachytili testovací charakteristiky všech postižených pacientů. Naše schopnost hodnotit ceruloplasmin jako diagnostický test byla omezená, protože jsme mohli zahrnout pouze měření, kde bylo provedeno definitivní potvrzující testování. Kromě toho je možné, že heterozygotní nosič, který jsme identifikovali, měl ve skutečnosti WD s méně závažným fenotypem., Vzhledem k tomu, že většina WD pacienti jsou složené heterozygoti a že existuje mnoho onemocnění-konkrétní mutace, to může být obtížné odlišit zdravé dopravce z postižené individual17. Rutinní screening všech pacientů má omezenou klinickou užitečnost a ceruloplasmin by neměl být používán jako součást empirické baterie testů tvořících jaterní obrazovku. Uvážlivější použití ceruloplazminu u vybrané populace s vyšší pravděpodobností před testem Wilsonovy choroby může zvýšit její užitečnost jako screeningového nástroje., Diagnostické bodovací systémy, jako je systém EASL11, mohou pomoci s stratifikací nebo kontextualizací nízkého výsledku ceruloplazminu v séru. Existuje jasná potřeba pro vyšší vzdělávání, pokud jde o vhodné označení pro ceruloplasmin testování všech odkazem klinických oborů, ale zejména non-neurolog a non-gastroenterologie zdrojů. Test výkonu může zlepšit s lokálně ověřené nižší referenční rozsahy, dodržování obecných zásad a použití ve více vyberte populace.,
Korespondence: S O ‚sullivan
Oddělení Neurologie, Cork University Hospital, Korek
Email:
finanční Prostředky
S O‘ sullivan získal podporu, aby se zúčastnili setkání Eisai Pharma, UCB, AbbVie, Lundbeck-Pharma a Teva Pharma
- Cauza E, Maier-Dobersberger T, Polli C, Kaserer K, Kramer L, Ferenci P. Screening u wilsonovy choroby u pacientů s jaterní onemocnění sérového ceruloplazminu. Žurnál hepatologie. 1997;27:358-62.
- Medici V, Rossaro L, Sturniolo GC. Wilsonova nemoc-praktický přístup k diagnostice, léčbě a sledování., Zažívací a jaterní onemocnění : úřední věstník italské Společnosti Gastroenterologie a italské Asociace pro Studium Jater. 2007;39:601-9.
- Roberts EA, Schilsky ml. Diagnostika a léčba Wilsonovy choroby: aktualizace. Hepatologie (Baltimore, Md). 2008;47:2089-111.
- Stremmel W, Meyerrose KW, Niederau C, Hefter H, Kreuzpaintner G, Strohmeyer g. Wilsonova choroba: klinická prezentace, léčba a přežití. Anály vnitřního lékařství. 1991;115:720-6.
- Hellman NE, Gitlin JD. Ceruloplazmin metabolismus a funkce. Roční přehled výživy., 2002;22:439-58.
- Scott J, Gollan JL, Samourian s, Sherlock s. Wilsonova choroba, prezentující se jako chronická aktivní hepatitida. Gastroenterologie. 1978;74:645-51.
- German Jl, 3rd, Bearn AG. Vliv estrogenů na metabolismus mědi u Wilsonovy choroby. Journal of clinical investigation. 1961;40:445-53.
- Mak CM, Lam CW, Tam S Diagnostickou přesnost sérového ceruloplazminu v Wilson onemocnění: stanovení senzitivity a specificity pomocí ROC analýzy křivky mezi ATP7B-genotyp jedinců. Klinická chemie. 2008;54:1356-62.,
- Ferenci P, Steindl-Mundo P., Vogel, W, Jessner W, Gschwantler M, Stauber R, Datz C, Hackl F, Wrba F, Bauer P., Lorenz, O. Diagnostické hodnoty kvantitativní poruchou stanovení mědi u pacientů s Wilsonovou Chorobou. Klinická gastroenterologie a hepatologie: oficiální časopis klinické praxe Americké gastroenterologické asociace. 2005;3:811-8.
- Shah AB, Černov jsem, Zhang HT, Ross BM, Das K, Lutsenko Y, Pavone L, Evgrafov O, Ivanova-Smolenskaya IA, Annerén G, Westermark K, Urrutia FH, Penchaszadeh GK, Sternlieb jsem, Scheinberg IH, Gilliam TC, Petrukhin K., Identifikace a analýza mutací v genu Wilsonovy choroby (ATP7B): populační frekvence, genotyp-fenotypová korelace a funkční analýzy. American journal of human genetics. 1997;61:317-28.
- pokyny pro klinickou praxi EASL: Wilsonova choroba. Žurnál hepatologie. 2012;56:671-85.
- Gow PJ, Smallwood RA, Angus PW, Smith AL, Wall AJ, Sewell RB. Diagnóza Wilsonovy choroby: zkušenost za tři desetiletí. Střevo. 2000;46:415-9.
- Tapper EB, Rahni DO, Arnaout R, Lai m. nadužívání měření ceruloplazminu v séru. American journal of medicine., 2013;126:926.e1-5.
- Goldstein IM, Kaplan HB, Edelsonem HS, Weissmann G. Ceruloplazminu: akutní fáze reaktantů, které uklízí kyslíku-odvozené volné radikály. Anály Newyorské akademie věd. 1982;389:368-79.
- Arredondo M, Nunez H, Lopez G, Pizarro F, Ayala M, Araya M. Vliv estrogenů na měď ukazatele: in vivo a in vitro studií. Výzkum biologických stopových prvků. 2010;134:252-64.
- Dufour JF, Kaplan mm. Muddying the water: Wilsonova nemoc brzy nezmizí. Gastroenterologie. 1997;113:348-50.
17. Schilsky ML, Ala a., Genetické testování Wilsonovy choroby: dostupnost a užitečnost. Aktuální gastroenterologické zprávy. 2010;12:57-61.
Strana 341
















Napsat komentář