US Pharm. 2010;35(5):36-41.
uma relação entre diabetes mellitus (DM) e demência é inegável, com numerosos estudos concluindo que DM aumenta o risco de declínio cognitivo e demência, incluindo a doença de Alzheimer (AD).1-5 DM não só aumenta o risco de demência, mas também aumenta a taxa de desenvolvimento de demência de duas a três vezes.,3 o mecanismo desta insuficiência não é totalmente compreendido, mas é colocada a hipótese de que a hiperglicemia, resistência à insulina, stress oxidativo, produtos finais avançados da glicação e citoquinas inflamatórias levam colectivamente a disfunção cognitiva.5 na verdade, a diabetes foi descrita como um” tipo especial de envelhecimento acelerado ” em 1976 devido às suas muitas complicações associadas.,5 a aparente sobreposição entre DM e demência levou à sugestão de que o AD não é apenas um distúrbio neurológico, mas sim um distúrbio neuroendócrino, com Steen et al cunhando o termo diabetes tipo 3 para descrever esta doença híbrida.,6
Visão geral de Insulina, Resistência/Tolerância diminuída à Glicose
Fisiopatologia: Os tolerância diminuída à glicose—definido como um plasma glucose de 140 mg/dL a 199 mg/dL depois de um teste oral de tolerância à glicose e alteração da glicose de jejum—definido como glicemia de jejum de 100 mg/dL e 125 mg/dL—diagnóstico de prediabetes (precursor do DM tipo 2 ), como é a hemoglobina A1C, de 5,7% para 6,4%.7 a fisiopatologia dos prediabetes é a mesma que a do T2DM, que é diagnosticada após um jejum de glucose sanguínea de 126 mg / dL ou superior ou de A1C de 6.,Igual ou superior a 5% (ensaio repetido para confirmação).Em ambas as condições, a resistência à insulina desenvolve-se nos tecidos periféricos, onde a insulina é necessária para a captação de glucose (nomeadamente músculo, fígado e gordura), e o pâncreas é forçado a fornecer cada vez mais insulina para superar esta resistência.Nesta fase, os doentes são frequentemente hiperinsulinémicos; no entanto, ao longo do tempo, o pâncreas não consegue satisfazer as exigências dos tecidos, e as células beta produtoras de insulina do pâncreas falham lentamente, produzindo cada vez menos insulina.,Sem insulina suficiente, as concentrações de glucose no sangue aumentam, levando a pré-diabetes e, em até 70% dos doentes com pré-diabetes, T2DM.As complicações da hiperglicemia são muitas e abrangem um risco aumentado de complicações macrovasculares (incluindo enfarte do miocárdio, acidente vascular cerebral e doença vascular periférica) e complicações microvasculares (incluindo nefropatia, neuropatia e retinopatia).Tratamento: existem muitas terapêuticas para tratar DM., O tratamento inicial para prédiabetes e T2DM é a modificação do estilo de vida envolvendo dieta, exercício e perda de peso.A Associação Americana da Diabetes (ADA) recomenda também a consideração da metformina em doentes com pré-diabetes com elevado risco de desenvolver diabetes.A metformina é recomendada como terapêutica farmacológica inicial para a T2DM.Muitas vezes, é necessária terapêutica farmacológica adicional para alcançar objetivos glicêmicos da ADA, incluindo um A1C
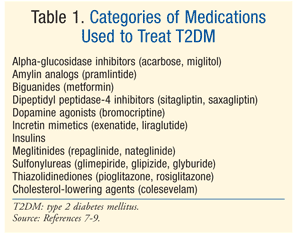
7%.,7 existem numerosas classes de medicação para T2DM (Tabela 1), e a escolha do agente para normalizar a glicose no sangue depende de uma série de fatores específicos do paciente e da medicação. É importante notar que muitos doentes com T2DM irão eventualmente necessitar de insulina exógena para atingir e manter a euglicemia à medida que a função das células beta diminui progressivamente.
Overview of AD
Pathophysiology: AD is the most common form of dementia in older adults, accounting for 60% to 80% of all cases.,Duas marcas histopatológicas de AD são placas neuríticas e tangles neurofibrilares.11 placas consistem em proteínas beta-amilóides insolúveis. Tangles, que são intracelulares, são compostos de proteína tau fosforilada. A proteína Tau é importante para a montagem de microtúbulos, e quando esta proteína é anormalmente fosforilada, a função neuronal é interrompida. Os neurónios neurofibrilares afectam mais frequentemente os neurónios colinérgicos.12 Além disso, a ruptura do principal neurotransmissor excitatório, o glutamato, contribui para a patologia do AD., Na AD, há uma sobreativação do glutamato, sinalizando um processo conhecido como excitotoxicidade, que leva à formação de placas, hiperfosforilação da proteína tau, e morte celular.Em resumo, a excitotoxicidade e a formação de placas neuríticas e tangles neurofibrilares perturbam as vias neurotransmissoras, resultando na aprendizagem e perda de memória associadas à AD.tratamento
: as terapêuticas farmacológicas para a AD aprovadas pela FDA estão resumidas na tabela 2.,11,12 embora ainda haja muito a aprender em relação a terapias que tratam ou alteram a patologia da AD, as terapias actualmente disponíveis envolvem o uso de inibidores da acetilcolinesterase, dos quais existem quatro, e o antagonista do receptor N-metil-d-aspartato Memantina.

a Insulina e o Cérebro
Embora seja necessário para o transporte de glicose em tecidos periféricos à insulina não parece ser necessário para o transporte de glicose para o cérebro ou para cerebral do metabolismo da glicose., Embora o transporte de glucose para o cérebro não seja dependente de insulina, a própria insulina é transportada através da barreira hemato–encefálica (BBB) por processos de transporte mediados pelo receptor de insulina.Este mecanismo de transporte é saturável; após períodos prolongados de concentrações excessivas de insulina (hiperinsulinemia) na periferia, tais como as observadas em prediabetes e T2DM, este mecanismo de transporte mediado pelo receptor diminui, reduzindo assim o transporte de insulina para o cérebro e o líquido cefalorraquidiano.,para além da insulina, o factor de crescimento tipo 1 (IGF-1), semelhante à insulina, está presente no cérebro e é necessário para o crescimento e a função normais do sistema nervoso central (SNC).14 receptores de insulina e IGF – 1 estão localizados em todo o cérebro em neurônios e astrócitos (células em forma de estrela no SNC que ajudam a suportar neurônios no cérebro). Duas áreas do cérebro que são cruciais para a aprendizagem e memória, o hipocampo e o hipotálamo, contêm altas concentrações de receptores de insulina.No rato, a administração intracerebroventricular de insulina demonstrou aumentar a memória.,Além disso, verificou-se que a administração de insulina intranasal no ser humano aumenta o desempenho da memória.Tal como anteriormente referido, a insulina não é necessária para o metabolismo da glucose cerebral; no entanto, podem existir áreas específicas no cérebro em que a insulina desencadeia processos metabólicos que envolvem glucose. Em estudos realizados no rato, a insulina demonstrou influenciar a utilização de glucose no hipotálamo e no locus coeruleus, duas áreas que são importantes para a aprendizagem e memória.,A aprendizagem também tem sido mostrado para facilitar o aumento da expressão dos receptores de insulina do SNC, levando à postulação de que a presença e atividade da insulina no cérebro contribuem e desempenham um papel essencial na aprendizagem e na memória. A insulina também pode contribuir para a modulação de neurotransmissores do SNC, notavelmente acetilcolina e norepinefrina, ambos críticos para a cognição normal e para a saúde cerebral.,18
resistência à insulina e demência visão geral
: parece haver muitos defeitos na sinalização de insulina no cérebro dos doentes com AD, levando a uma diminuição da utilização de glucose e do metabolismo energético.Como o T2DM está associado à resistência periférica à insulina, A AD está associada à resistência à insulina cerebral.No início da publicidade, parece haver uma captação inadequada de insulina e sinalização no cérebro, um sinal de resistência à insulina.5.19. 21. 22 aumento dos receptores de insulina foram observados no cérebro de doentes com AD, provavelmente como compensação pela resistência à insulina.,Globalmente, esta diminuição na sinalização de insulina tem muitos efeitos a jusante na AD. Uma teoria é que baixas concentrações de insulina no SNC causam uma diminuição nos níveis de acetilcolina e fluxo sanguíneo cerebral.Adicionalmente, as alterações nas concentrações de insulina podem promover a formação de beta-amilóides e de proteínas tau.2 no cérebro, a enzima de degradação da insulina (IDE) está envolvida na degradação e depuração de proteínas beta-amilóides.Níveis elevados de insulina inibem a IDE e podem conduzir a uma diminuição da depuração beta-amilóide, aumentando subsequentemente a deposição cerebral de beta-amilóide.,Recentemente, ceramidas, uma família de lípidos, chamaram a atenção para o seu potencial papel na resistência à insulina e na demência.23,24 Ceramidas são geradas na presença de inflamação, que é comum na obesidade, T2DM, e AD.Uma vez que a ceramida atravessa rapidamente o BBB, A exposição causa alterações no metabolismo energético e na expressão do gene da insulina, contribuindo para a resistência à insulina.23, 24 esta é actualmente uma área de interesse activa, com investigadores que demonstram que a inibição da síntese da ceramida impediu a resistência à insulina mediada pela obesidade.,Insulina Intranasal: como mencionado anteriormente, a administração de insulina intranasal melhora o desempenho da memória no ser humano.Foram realizados vários estudos com insulina intranasal. Após a administração de 20 unidades de insulina intranasal duas vezes por dia a indivíduos humanos, Reger et al descobriu que, em comparação com o placebo, o grupo tratado com insulina reteve mais informação verbal e mostrou maior atenção e estado funcional.,Estes investigadores também observaram que a glucose plasmática em jejum e a insulina não se alteraram com o uso de insulina intranasal, indicando que a administração intranasal proporciona acesso directo à insulina do SNC sem efeitos periféricos.Agonistas PPAR-Gama: extensivamente estudados para o tratamento da resistência à insulina periférica, as tiazolidinedionas rosiglitazona e pioglitazona estão a ser investigadas pelo seu papel no tratamento da AD. As tiazolidinedionas são agonistas do receptor-gama activado pelo proliferador de peroxisomas., O PPAR-gama está envolvido no metabolismo da glucose e dos lípidos e modula a inflamação, um contribuinte conhecido para a AD.22,27 as tiazolidinedionas são sensibilizantes da insulina, trabalhando para reduzir a resistência à insulina; também parecem diminuir a inflamação.Em vários ensaios controlados com placebo, os doentes tratados com rosiglitazona apresentaram melhoria da memória e da função cognitiva.Apesar de terem sido realizados apenas pequenos estudos com pioglitazona, esta medicação também tem sido associada a melhorias na memória e cognição.,Apesar da pioglitazona e da rosiglitazona terem fraca permeabilidade BBB, cada um destes fármacos foi documentado no cérebro após administração oral.22 Embora estes medicamentos podem desempenhar um papel na prevenção ou tratamento de ANÚNCIO, que não são atualmente aprovados pela FDA para pacientes com AD, e os seus potenciais benefícios e riscos devem ser cuidadosamente consideradas numa base individual.exercício aeróbico: talvez o método mais eficaz e mais negligenciado de reduzir a resistência à insulina seja a actividade física., A obesidade tem sido associada a um risco aumentado de resistência à insulina, diabetes, demência e AD.O exercício físico melhora a sensibilidade à insulina e reduz os níveis de insulina periférica.26,31 atividade física, independente do peso, está associada a um menor risco de AD, tornando-se a única terapia neuroprotetora comprovada.29-31 um possível mecanismo desta neuroprotecção é que o exercício promove a depuração de proteínas beta-amilóides e aumenta o fator neurotrófico derivado do cérebro, um fator de crescimento vital para a cognição e sobrevivência neuronal que é reduzida em AD.,32 O papel do farmacêutico os farmacêuticos desempenham um papel essencial na educação dos doentes sobre novas terapias; também precisam de se manter a par de novas descobertas ou condições médicas que são frequentemente apresentadas nas notícias. A diabetes tipo 3 é uma dessas doenças. Embora ainda haja muito a aprender sobre esta potencial nova ligação entre diabetes e cognição deficiente, o público irá perguntar a opinião dos seus prestadores de cuidados de saúde. Além disso, muitos pacientes com diabetes estarão interessados em aprender mais e recorrerão aos seus farmacêuticos para obter informações., Portanto, os farmacêuticos devem discutir a compreensão atual desta condição com seus pacientes e também aconselhá-los sobre estratégias que podem diminuir o seu risco, dadas as suas co-morbilidades individuais.
conclusão
estudo intensivo está em curso numa tentativa de melhor caracterizar a diabetes tipo 3 e desenvolver estratégias preventivas e terapêuticas. Até à data, não existem tratamentos específicos com eficácia comprovada na prevenção do declínio cognitivo ou da DM em doentes com DM., Assim, o tratamento do compromisso cognitivo em doentes com DM é idêntico ao dos doentes sem DM, com atenção específica ao controlo glicémico e aos factores de risco cardiovascular. Esta é a mesma abordagem já essencial para prevenir complicações relacionadas com o DM. Embora alguns grupos de doentes pareçam estar em maior risco de disfunção cognitiva, a maioria dos doentes com DM não tem associações clínicas bem definidas., Embora não existam opções de tratamento específicas disponíveis, a abordagem lógica atual é atingir o controle glicêmico e gerir prudentemente os fatores de risco cardiovascular, tais como hiperlipidemia e hipertensão.1. Stewart R, Liolitsa D. diabetes mellitus tipo 2, perturbações cognitivas e demência. Diabet Med.
2. Xu WL, von Strauss e, Qiu CX, et al. A diabetes não controlada aumenta o risco de doença de Alzheimer: um estudo de coorte baseado na população. Diabetologia. 2009;52:1031-1039.
3. Arvanitakis Z, Wilson RS, Bennett DA. Diabetes mellitus, demência e função cognitiva em pessoas mais velhas., J Nutr Envelhecimento Da Saúde. 2006;10:287-291.
4. Jacobson AM, Musen G, Ryan CM, et al. Efeito a longo prazo da diabetes e do seu tratamento na função cognitiva. N Engl J Med. 2007;356:1842–1852.
5. Whitmer RA. Diabetes tipo 2 e risco de disfunção cognitiva e demência. Curr Neurol Neurosci Rep. 2007; 7: 373-380.
6. Steen E, Terry BM, Rivera EJ, et al. Alteração da expressão do factor de crescimento da insulina e insulina e mecanismos de sinalização na doença de Alzheimer—é este tipo de diabetes? J Alzheimers Dis. 2005;7:63-80.
7. Associação Americana De Diabetes. Standards of medical care in diabetes-2010., Cuidados Com A Diabetes.
8. Triplitt Cl, Reasner CA, Isley WL. Diabetes mellitus. In: DiPiro JT, Talbert RL, Yee GC, et al, eds. Princípios de farmacoterapia prática. 7th ed. New York, NY: McGraw Hill Medical; 2008:1205-1241.
9. Nathan DM, Buse JB, Davidson MD, et al. Medical management of hyperglicemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy: a consensus statement of the American Diabetes Association and the European Association for the Study of Diabetes. Cuidados Com A Diabetes.
10. Hebert LE, Scherr PA, Bienias JL, et al., Alzheimer disease in the US population: prevalence estimates using the 2000 census. Arch Neurol. 2003;60:1119-1122.
11. Cummings J. Alzheimer disease. N Engl J Med. 2004;351:56-67.
12. Slattum PW, Swerdlow RH, Hill AM. Doença de Alzheimer. In: DiPiro JT, Talbert RL, Yee GC, et al, eds. Princípios de farmacoterapia prática. 7th ed. New York, NY: McGraw Hill Medical; 2008:1051-1065.
13. Craft S, Watson GS. Insulina e doença neurodegenerativa: mecanismos comuns e específicos. Lancet Neurol. 2004;3:169-178.
14. De La Monte SM, Wands JR., Review of insulina and insuline-like growth factor expression, signaling, and malfunction in the central nervous system: relevance to Alzheimer disease. J Alzheimers Dis. 2005;7:45-61.
15. Park CR, Seeley RJ, Craft s, Woods SC. A insulina Intracerebroventricular aumenta a memória numa tarefa de prevenção passiva. Physiol Behav. 2000;68:509-514.
16. Fehm HL, Perras B, Smolnik R, et al. Manipulação de vias neuropeptidergicas em humanos: uma nova abordagem à Neurofarmacologia? EUR J Farmacol. 2000;405:43-54.
17. Zhao WQ, Alkon DL. Papel da insulina e do receptor de insulina na aprendizagem e memória., Endocrinol De Células Moles. 2001;177:125-134.
18. Kopf s, Baratti C. efeitos da administração pós-formação de insulina na retenção de uma resposta de habituação nos ratinhos: participação de um mecanismo colinérgico central. Neurobiol Aprende Mem.
19. Revill P, Moral MA, Prous JR. sinais de insulina debilitados e a patogênese da doença de Alzheimer. Drogas Hoje (Barc). 2006;42:785-790.
20. Moroz n, Tong M, Longato L, et al. Neurodegeneração limitada do tipo Alzheimer em obesidade experimental e diabetes mellitus tipo 2. J Alzheimers Dis. 2008;15:29-44.
21. Haan MN., Visão terapêutica: diabetes mellitus tipo 2 e o risco de aparecimento tardio da doença de Alzheimer. Nat Clin Prat Neurol. 2006;2:159-166.
22. Landreth G, Jiang Q, Madrekar S, et al. Ppargamma agonista como terapêutica para o tratamento da doença de Alzheimer. Neurotherapeutics. 2008;5:481-489.
23. Lyn-Cook LE, Lawton M, Tong M, et al. A ceramida hepática pode mediar resistência à insulina cerebral e neurodegeneração na diabetes tipo 2 e esteatohepatite não alcoólica. J Alzheimers Dis.
24. Tong M, de La Monte SM. Mecanismos de neurodegeneração mediada pela ceramida. J Alzheimers Dis.
25., Reger MA, Watson GS, Green PS. A insulina Intranasal melhora a cognição e modula a beta-amilóide no início da DC. Neurologia. 2008;70:440-448.
26. Craft S. síndrome de resistência à insulina e doença de Alzheimer: efeitos relacionados com a idade e a obesidade na memória, amilóide e inflamação. Envelhecimento Neurobiol. 2005; 26(suppl 1): 65-69.
27. Jiang Q, Heneka M, Landreth GE. O papel do receptor-gama activado pelo proliferador de peroxissoma (PPARgamma) na doença de Alzheimer: implicações terapêuticas. Drogas do SNC. 2008;22:1-14.
28. Watson GS, Cholerton BA, Reger MA, et al., A cognição preservada em doentes com doença de Alzheimer precoce e compromisso cognitivo ligeiro amnésico durante o tratamento com rosiglitazona: um estudo preliminar. Sou J Geriatr Psychiatry. 2005;13:950-958.
29. Luchsinger JA, Mayeux R. Adiposity and Alzheimer disease. Curr Alzheimer Res. 2007; 4: 127-134.
30. Whitmer RA. A epidemiologia da adiposidade e demência. Curr Alzheimer Res. 2007; 4: 117-122.
31. Watson GS, Craft S. O papel da resistência à insulina na patogénese da doença de Alzheimer: implicações para o tratamento. Drogas do SNC. 2003;17:27-45.
32. Cole GM, Frautschy SA., O papel da insulina e do fator neurotrófico sinalizando o envelhecimento cerebral e a doença de Alzheimer. Exp Gerontol. 2007;42:10-21.
















Deixe uma resposta