온도가 증가함에 따라 그렇게 평가 효소 반응입니다. 섭씨 10 도의 온도 상승은 대부분의 효소의 활성을 50%~100%증가시킵니다. 1 도 또는 2 도 정도의 작은 반응 온도의 변화는 결과에서 10%내지 20%의 변화를 도입 할 수있다. 이 증가는 상승 된 온도가 효소의 구조를 깨뜨릴 때까지만 특정 시점까지입니다. 일단 효소가 변성되면 고칠 수 없습니다., 각 효소는 아미노산과 펩타이드 사이의 구조와 결합이 다르므로 변성을위한 온도는 각 효소에 특이적입니다. 기 때문에 대부분의 동물 효소는 빠르게 변성에서 이상의 온도 40°C,가장 효소 판정을 수행되는 약간 아래의 온도.
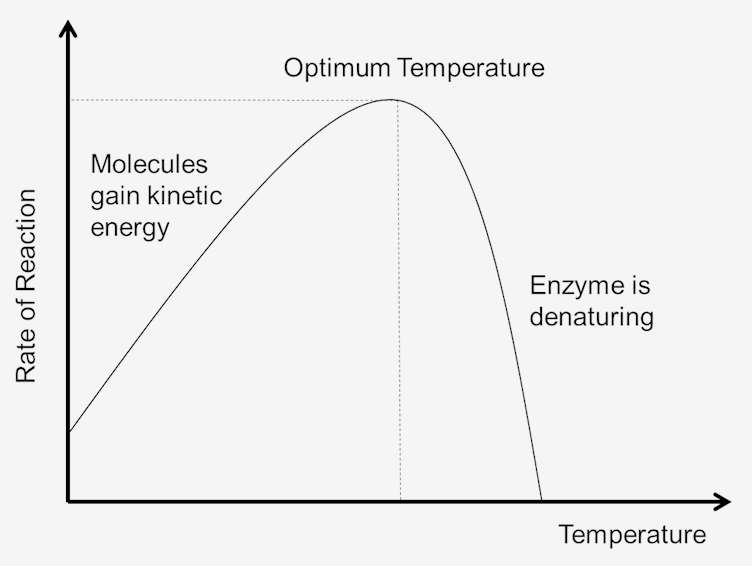 그림 1. 반응 속도에 대한 온도의 영향.
그림 1. 반응 속도에 대한 온도의 영향.
일정 기간 동안 효소는 적당한 온도에서도 비활성화 될 것입니다. 5°C 이하에서 효소를 저장하는 것이 일반적으로 가장 적합합니다. 온도가 낮을수록 화학 반응이 느려집니다., 효소들이 결국이 비활성화에 냉동 온도나 복원들의 대부분의 효소 활동을 때 온도를 다시 증가하는 동안,몇 가지 효소들을 잃은 그들의 활동을 때 냉동입니다.
운동 에너지 및 내부 에너지
의 온도를 시스템이 어느 정도의 측정의 운동에너지에 있는 분자 시스템입니다. 모든 분자 사이의 충돌은 온도가 증가함에 따라 증가합니다. 이것은 온도 상승에 따른 속도 및 운동 에너지의 증가 때문입니다. 빠른 속도로,충돌 사이의 적은 시간이 될 것입니다., 이로 인해 더 많은 분자가 활성화 에너지에 도달하여 반응 속도가 증가합니다. 분자도 더 빨리 움직이기 때문에 효소와 기질 사이의 충돌도 증가합니다. 따라서 더 낮은 운동 에너지,낮은 온도 시스템의하고,마찬가지로,더 높은 운동 에너지,큰의 온도 시스템입니다.시스템의 온도가 증가함에 따라 시스템의 분자의 내부 에너지가 증가합니다., 내부에너지의 분자 포함할 수 있는 에너지 변환,진동 에너지 및 에너지 회전의 분자,관련된 에너지에서의 화학적 결합의 분자뿐만 아니라 에너지에 관련된 nonbonding 상호 작용합니다. 이 열의 일부는 화학 포텐셜 에너지로 변환 될 수 있습니다. 는 경우에는 이 화학 잠재적 에너지가 증가 충분의 일부 채권이 약한 결정하는 세 가지 차원 모양의 활성 단백질이 고장난 것일 수 있습니다. 이것은 단백질의 열 변성을 초래할 수 있고 따라서 단백질을 불 활성화시킬 수있다., 따라서 너무 많은 열을 발생시킬 수 있을 평가하는 효소의 촉매 반응하기 때문에 감소하는 효소 또는 기판된 변성 및 비활성화됩니다.
최적의 온도
각 효소는 온도 범위에는 최대 속도의 반응이 달성된다. 이 최대 값은 효소의 온도 최적 값으로 알려져 있습니다. 대부분의 효소의 최적 온도는 화씨 약 98.6 도(섭씨 37 도)입니다. 더 낮은 온도와 더 높은 온도에서 잘 작동하는 효소도 있습니다., 예를 들면,북극의 동물은 효소를 낮추는 최적의 온도;동물 사막에서 효소가 있는 기후에 적응하는 더 높은 온도. 그러나 효소는 여전히 단백질이며 모든 단백질과 마찬가지로 화씨 104 도 이상의 온도에서 분해되기 시작합니다. 따라서 효소 활성의 범위는 효소가 활성화되기 시작하는 온도와 단백질이 분해되기 시작하는 온도에 의해 결정됩니다.,
관련 서비스
효소 반응 속도
Enzymology 분석 실험
을 논의 서비스를 더 세부 정보,저희에게 연락하십시오를 호출하여 1-631-562-8517,또는 e-링 [email protected].
















답글 남기기