lämpötilan noustessa samoin entsyymireaktioiden nopeus. Kymmenen asteen lämpötilan nousu lisää useimpien entsyymien aktiivisuutta 50-100 prosenttia. Jopa 1 tai 2 asteen reaktiolämpötilan vaihtelut voivat aiheuttaa 10-20 prosentin muutoksia tuloksissa. Tämä nousu on vain tiettyyn pisteeseen asti, kunnes kohonnut lämpötila rikkoo entsyymin rakenteen. Kun entsyymi on denaturoitu, sitä ei voida korjata., Koska kukin entsyymi on rakenteeltaan erilainen ja aminohappojen ja peptidien välinen sidos, denaturointilämpötila on kullekin entsyymille spesifinen. Koska useimmat eläinten entsyymit nopeasti tullut denaturoitu lämpötiloissa yli 40°C, suurin entsyymin määritykset tehdään hieman alle tuon lämpötilan.
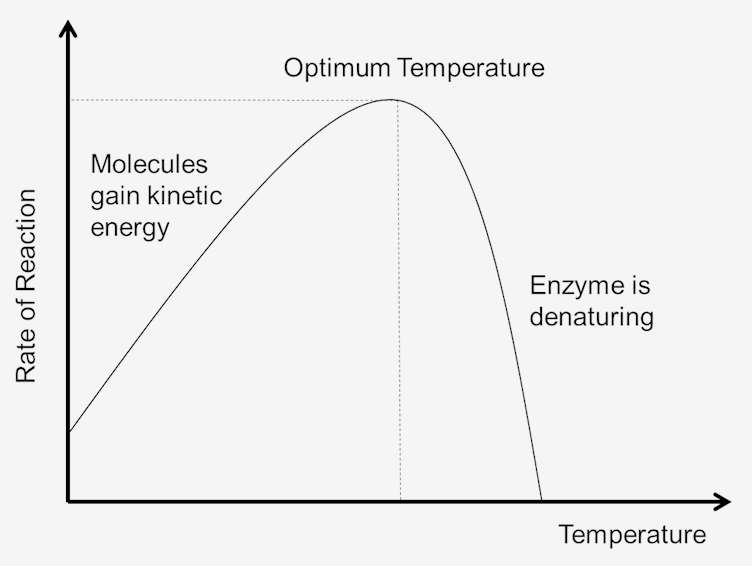 Kuva 1. Lämpötilan vaikutus reaktionopeuteen.
Kuva 1. Lämpötilan vaikutus reaktionopeuteen.
tietyn ajan kuluessa entsyymit deaktivoituvat jopa kohtalaisissa lämpötiloissa. Entsyymien säilytys 5°C: ssa tai sen alapuolella on yleensä sopivin. Matalammat lämpötilat johtavat hitaampiin kemiallisiin reaktioihin., Entsyymien tulee lopulta aktiivinen pakkasella, mutta palauttaa suurimman osan entsyymin toimintaa, kun lämpötila kasvaa jälleen, kun taas jotkut entsyymit menettävät toimintaa, kun jäädytetty.
Kineettinen Energia ja Energian
lämpötila-järjestelmä on jossain määrin mitta kineettinen energia molekyylejä järjestelmässä. Kaikkien molekyylien väliset törmäykset lisääntyvät lämpötilan noustessa. Tämä johtuu lämpötilan nousua seuraavan nopeuden ja liike-energian kasvusta. Nopeammilla nopeuksilla törmäysten välillä on vähemmän aikaa., Tällöin aktivaatioenergiaan pääsee enemmän molekyylejä, mikä lisää reaktioiden nopeutta. Koska molekyylit myös liikkuvat nopeammin, myös entsyymien ja substraattien väliset törmäykset lisääntyvät. Näin ollen mitä pienempi liike-energia, alempi lämpötila-järjestelmä, ja, lisäksi, sitä suurempi liike-energia, sitä suurempi lämpötila-järjestelmän.
systeemin lämpötilan noustessa järjestelmän molekyylien sisäinen energia kasvaa., Sisäinen energia molekyylejä voi sisältää translaation energiaa, värähtelyenergiaa ja rotaatio energia molekyylejä, energiaa mukana kemiallisten liimaus molekyylien sekä energian mukana nonbonding vuorovaikutusta. Osa tästä lämmöstä voidaan muuntaa kemialliseksi potentiaalienergiaksi. Jos tämä kemiallinen potentiaalienergian kasvu on tarpeeksi suuri osa heikoista sidoksista, jotka määrittävät aktiivisten proteiinien kolmiulotteisen muodon, voi rikkoutua. Tämä voi johtaa proteiinin termiseen denaturaatioon ja siten inaktivoida proteiinin., Liika kuumuus voi siis aiheuttaa entsyymin katalysoiman reaktion hidastumisen, koska entsyymi tai substraatti denaturoituu ja inaktiiviseksi.
optimilämpötila
jokaisella entsyymillä on lämpötila-alue, jolla saavutetaan suurin reaktionopeus. Tämä maksimi tunnetaan entsyymin lämpötilaoptimaalina. Useimpien entsyymien optimaalinen lämpötila on noin 98,6 astetta. On myös entsyymejä, jotka toimivat hyvin alemmissa ja korkeammissa lämpötiloissa., Esimerkiksi arktisten eläinten entsyymit ovat sopeutuneet alhaisempiin optimaalisiin lämpötiloihin; aavikkoilmaston eläimillä on korkeampiin lämpötiloihin sopeutuneita entsyymejä. Entsyymit ovat kuitenkin edelleen proteiineja, ja kaikkien proteiinien tavoin ne alkavat hajota yli 104 asteen lämpötiloissa. Siksi erilaisia entsyymin aktiivisuus määritetään lämpötila, jossa entsyymi alkaa aktivoida ja lämpötila, jossa proteiini alkaa hajota.,
Liittyvät Palvelut
entsyymikinetiikka
Enzymology Määritykset
keskustella enemmän palvelun yksityiskohtia, ota meihin yhteyttä soittamalla 1-631-562-8517, tai e-mailing us at [email protected].
















Vastaa